题目内容
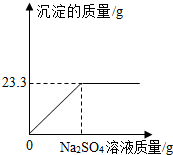 称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl)
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl)(1)完全反应后生成BaSO4沉淀
(2)恰好完全反应时消耗Na2SO4溶液的质量是
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据图示可以判断出生成的沉淀硫酸钡的质量;
(2)设出硫酸钠溶液的质量,然后根据硫酸钡沉淀的质量及反应反应方程式计算出完全反应时消耗Na2SO4溶液的质量;
(3)所得溶液中溶质的质量分数=
×100%,溶质是氯化钠,包括原混合物中的氯化钠(根据沉淀的质量求出氯化钡的质量,再用混合物的质量-氯化钡质量)和反应生成的氯化钠(根据沉淀的质量可求出),所得溶液的质量=所加的所有物质的总质量-生成沉淀的质量.
(2)设出硫酸钠溶液的质量,然后根据硫酸钡沉淀的质量及反应反应方程式计算出完全反应时消耗Na2SO4溶液的质量;
(3)所得溶液中溶质的质量分数=
| 溶质质量 |
| 所得溶液质量 |
解答:解:
(1)由图示可知,生成沉淀的最大量为23.3g,所以完全反应生成硫酸钡沉淀的质量为23.3g,
故答案为:23.3;
(2)设BaCl2的质量为x,反应生成的NaCl的质量为y;恰好完全反应时消耗Na2SO4的质量为z
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 142 233 117
x z 23.3g y
=
=
x=20.8g
y=11.7g
=
z=14.2g
(2)恰好完全反应时消耗Na2SO4溶液的质量是
=142g
(3)恰好完全反应后所得溶液中溶质的质量分数:
×100%=9.3%;
答案:
(1)23.3
(2)142
(3)9.3%;
(1)由图示可知,生成沉淀的最大量为23.3g,所以完全反应生成硫酸钡沉淀的质量为23.3g,
故答案为:23.3;
(2)设BaCl2的质量为x,反应生成的NaCl的质量为y;恰好完全反应时消耗Na2SO4的质量为z
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 142 233 117
x z 23.3g y
| 208 |
| x |
| 233 |
| 23.3g |
| 117 |
| y |
x=20.8g
y=11.7g
| 142 |
| z |
| 233 |
| 23.3g |
z=14.2g
(2)恰好完全反应时消耗Na2SO4溶液的质量是
| 14.2g |
| 10% |
(3)恰好完全反应后所得溶液中溶质的质量分数:
| 11.7g+(32.5g-20.8g) |
| 32.5g+100g+142g-23.3g |
答案:
(1)23.3
(2)142
(3)9.3%;
点评:求反应后所得溶液的质量的方法一般是用所加的所有物质的质量总和-生成气体的质量-生成沉淀的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分类是化学研究常用的方法.下列对物质分类正确的是( )
| A、空气和冰水混合物都属于混合物 |
| B、氧气和臭氧都属于单质 |
| C、碳酸钙和甲烷都属于有机物 |
| D、火碱和纯碱都属于碱 |
用分子的相关知识解释下列生活中的现象,其中错误的是( )
| A、“酒香不怕巷子深”,说明分子在不停运动 |
| B、分子由原子构成,说明分子比原子大 |
| C、20mL酒精和20mL水混合后体积小于40mL,说明分子间有间隙 |
| D、湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快 |
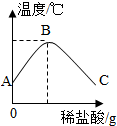 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示: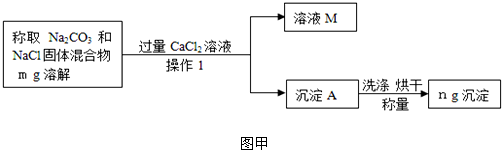
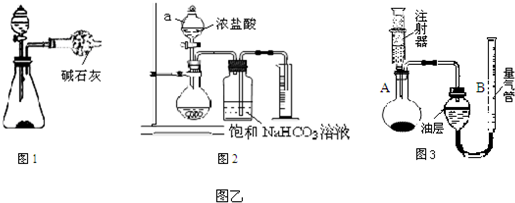
 人体中铁元素主要存在于血液中,是血红蛋白的成分,能帮助氧气的运输.如果体内缺铁会引起贫血.如图是某品牌补铁剂的药品标签.请回答:
人体中铁元素主要存在于血液中,是血红蛋白的成分,能帮助氧气的运输.如果体内缺铁会引起贫血.如图是某品牌补铁剂的药品标签.请回答:
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.