��Ŀ����
����Ŀ���������������������������������ء���ش�
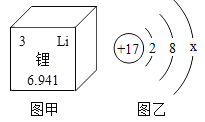
��1��������Ʒ�У���Ҫ���ý��������Ե���_____������ĸ����
A ������Ʒ B ���� C ������
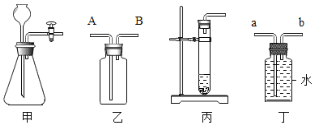
��2��Ϊ����֤����ͭ�������ֽ����Ļ��˳���������ַ����п��е���_____������ţ���
�����������ֱ���뵽����ͭ��Һ��
�������ֱ���뵽������������ͭ��Һ��
����ͭ�����ֱ���뵽��������Һ��
����ͭ�ֱ���뵽����������������Һ��
��3�����Ȼ�ͭ���Ȼ������Ļ����Һ�м���һ������þ�ۣ���ַ�Ӧ����ˣ��õ���������Һ������Һ��һ�����е�������_____���ѧʽ�������������еμ�ϡ���ᣬ�����ݲ�������������һ�����е�������_____���ѧʽ����
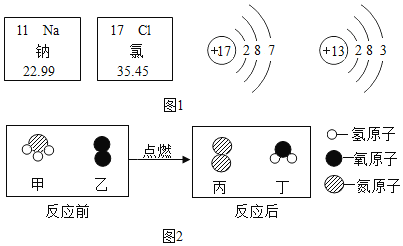
��4��������ԭ����һ����̼���������ڸ��������·�Ӧ�������Ͷ�����̼��д���÷�Ӧ�Ļ�ѧ����ʽ_____��
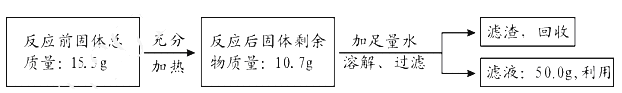
��5��¶����õĸ����������⣬��������ʵ������������е�_____������ѧӦ������ȥ���������ϡ������д���÷�Ӧ�Ļ�ѧ����ʽ_____��
��6����ҵ�����г���10%��ϡ������������Ʒ��������⣬ʵ������Ҫ���Ƹ�����200g����������Ͳ��ȡ������������Ϊ38%��Ũ���ᣨ�ܶ�Ϊ1.19g/mL��______mL��������������0.1����ʵ����������10%��ϡ����Ĺ����У������õ���Ͳ����ͷ�ι��⣬����Ҫ�õ��IJ�������������_____��
��7��ij������ÿ��������4900 t��Fe2O3 76%�ij�����ʯ���ó������Ͽ��ղ���Fe 98%��������������_____t��
���𰸡�C �٢� MgCl2 Fe��Cu 3CO+Fe2O3![]() 2Fe+3CO2�� ������ˮ Fe2O3+6HCl��2FeCl3+3H2O 44.2 �ձ��������� 2660
2Fe+3CO2�� ������ˮ Fe2O3+6HCl��2FeCl3+3H2O 44.2 �ձ��������� 2660
��������
��1�����Ƴɵ����������˽����ĵ����ԣ����C��
��2������������ͭ��Ӧ������֤���Ļ�Ա�ͭǿ����������ͭ����Ӧ����֪���Ļ�Ա�ͭ��������֤����ͭ�������ֽ����Ļ��˳�����ǿ��еķ�����
������������������ͭ����������Ӧ������֤����ͭ�Ļ�Ա���ǿ���뵫������֤����ͭ�Ļ�ԣ�������֤����ͭ�������ֽ����Ļ��˳�����Dz����еķ�����
��ͭ����������������������Ӧ������֤���Ļ�Ա�ͭ����ǿ����������֤ͭ�����Ļ�ԣ�������֤����ͭ�������ֽ����Ļ��˳�����Dz����еķ�����
��ͭ������������Ӧ����֪ͭ�Ļ�Ա�������ͭ����������Ӧ������֤ͭ�Ļ�Ա���ǿ������֤����ͭ�������ֽ����Ļ��˳�����ǿ��еķ���������٢���
��3�����Ȼ�ͭ���Ȼ������Ļ����Һ�м���һ������þ�ۣ���ַ�Ӧ����ˣ��õ���������Һ��������þ�Ļ����Դ���ͭ�����������Ȼ�ͭ���Ȼ�������Ӧ������Һ��һ�����е�������MgCl2������ȷ���Ȼ�ͭ���Ȼ������Ĵ��ڣ������������еμ�ϡ���ᣬ�����ݲ�������������һ�����е�������Fe�������û�����Cu��Mg����ȷ���Ƿ���ڡ����MgCl2��Fe��Cu��
��4��һ����̼���������ڸ��������·�Ӧ�������Ͷ�����̼�����3CO+Fe2O3![]() 2Fe+3CO2��
2Fe+3CO2��
��5��¶����õĸ����������⣬��������ʵ������������е�������ˮ������ѧ��Ӧ���������Ҫ�ɷ����������������������ᷴӦ�����Ȼ�����ˮ�����������ˮ����O2��H2O����Fe2O3+6HCl��2FeCl3+3H2O��
��6����������Ͳ��ȡ������������Ϊ38%��Ũ���ᣨ�ܶ�Ϊ1.19g/mL�������Ϊx��
����ϡ��ǰ����Һ�е��������������У�
200g��10%��1.19g/mL��x��38%��
��ã�x��44.2 mL��
ʵ����������10%��ϡ����Ĺ����У������õ���Ͳ����ͷ�ι��⣬����Ҫ�õ����������ձ��������������44.2���ձ�����������
��7����ó������Ͽ��ղ���Fe 98%��������������x����
![]()

![]()
x��2660t
���2660��

����Ŀ��ijʵ��С�����÷�����Һ�Ʊ�K2SO4
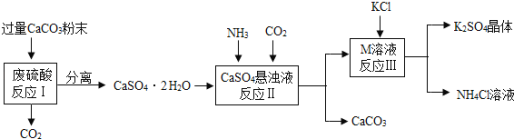
��1����CaCO3�гɷ�ĩ��Ŀ���� ��
��2�����������п�ѭ��ʹ�õ�������CO2�� ����д��ѧʽ����
��3����Ӧ����������ʵ��ܽ�����±�������Ϊ��Ӧ���ڳ�������ʵ�ֵ�ԭ����
���� | KCl | K2SO4 | NH4Cl | M |
�ܽ��/g��25���� | 34.0 | 11.1 | 37.2 | 19.5 |
��4������ˮ���ñ���K2SO4��Һϴ�ӷ�Ӧ�����þ����Ŀ���� ��Ϊ����˾����Ƿ�ϴ�Ӹɾ�����ȡ���һ��ϴ��Һ���ȼ��� ��ѡ����ţ���ͬ���������ã������ϲ���Һ�еμ� ���۲������жϣ�
a��AgNO3��Һ b��������BaCl2��Һ c��������Ba��NO3��2��Һ