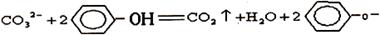9.(13分)A-E五种元素中,除A、B外其他均为短周期元素,它们的性质或原子结构如下表:
|
元素 |
元素性质或原子结构 |
|
A |
 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
|
B |
单质为生活中常见的金属,其相对原子质量比A大8 |
|
C |
地壳中含量最多的金属元素 |
|
D |
元素的主族序数是其所在周期序数的3倍 |
|
E |
E的某种原子的原子核内没有中子 |
(1)请写出A在元素周期表中的位置 ;C单质在强碱溶液反应的离子方程式是 。
 (2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a
kJ热量,此反应的热化学方程式是
。
(2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a
kJ热量,此反应的热化学方程式是
。
 ②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
。
②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
。

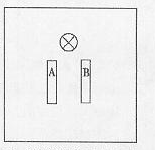 (3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、
(3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、
 B两种金属,插入含大量E+的电解质溶液的烧杯中,
B两种金属,插入含大量E+的电解质溶液的烧杯中,
 可组成原电池。
可组成原电池。
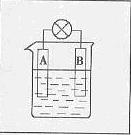
 请在右侧方框内相应位置上画出烧杯等,完成原电池电
请在右侧方框内相应位置上画出烧杯等,完成原电池电
 极与用电器连接的示意图。
极与用电器连接的示意图。
 (4)向2mL
0.5mol/L的Acl3溶液中加入3mL 3mol/L KF溶液,
(4)向2mL
0.5mol/L的Acl3溶液中加入3mL 3mol/L KF溶液,
 ACl2溶液褪成无色,再加入KI溶液和CCl4振荡后静置,
ACl2溶液褪成无色,再加入KI溶液和CCl4振荡后静置,
 CCl4层不显色,则下列说法正确的是(已知氧化性
CCl4层不显色,则下列说法正确的是(已知氧化性
 Fe3+>I2)
(填字母)。
Fe3+>I2)
(填字母)。
 a. A3+不与I-发生反应 b.
A3+与F-结合生成不与I-反应的物质
a. A3+不与I-发生反应 b.
A3+与F-结合生成不与I-反应的物质
 c. F-使I-的氧化性减弱 d.
A3+被F-还原为A2+,使溶液中不再存在A3+
c. F-使I-的氧化性减弱 d.
A3+被F-还原为A2+,使溶液中不再存在A3+
5. 几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( B )
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( B )
|
元素代号 |
A |
B |
D |
E |
G |
X |
Y |
Z |
|
化合价 |
-1 |
-2 |
+4、-4 |
-1 |
+5、-3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.099 |
0.110 |
0.143 |
0.160 |
0.186 |
A.A元素的单质能将E单质从XE3的溶液中置换出来

 B.A、X、Z的离子半径由大到小顺序是A->Z+>X3+
B.A、X、Z的离子半径由大到小顺序是A->Z+>X3+
 C.G元素的单质不存在同素异形体
C.G元素的单质不存在同素异形体
 D.Y元素的单在DB2中燃烧生成两种化合物
D.Y元素的单在DB2中燃烧生成两种化合物
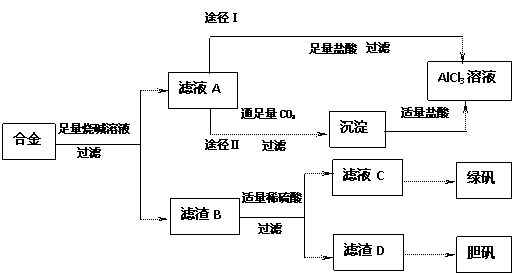
 (13分)
(13分)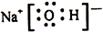 H-O-H
H-O-H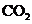
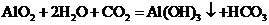 或
或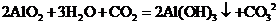
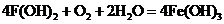
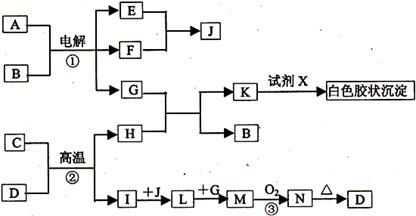
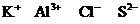 B.
B.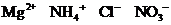
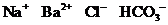 D.
D.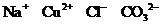
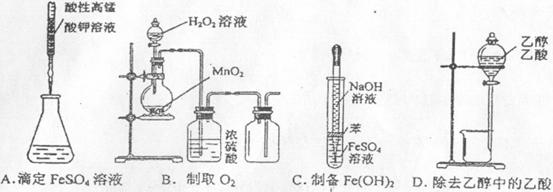
 A.
A.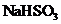 的水溶液显酸性,其原因是
的水溶液显酸性,其原因是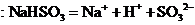
 B.在
B.在 溶液中逐滴滴入
溶液中逐滴滴入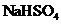 溶液至
溶液至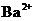 恰好完全沉淀时
恰好完全沉淀时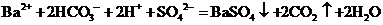
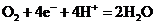
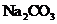 溶液中滴入过量的苯酚水溶液
溶液中滴入过量的苯酚水溶液