2.盐类水解规律
有弱才水解,无弱不水解;越弱越水解,都弱双水解;谁强显谁性,同强显中性。
|
盐的类型 |
实例 |
是否水解 |
离子的水解 |
溶液的pH |
|
强酸强碱盐 |
NaCl、KNO3 BaCl2 |
不水解 |
|
pH=7 |
|
强酸弱碱盐 |
NH4Cl、CuSO4 Fe(NO3)3 |
水解 |
NH4+、Cu2+ Fe3+ |
pH<7 |
|
强碱弱酸盐 |
KClO、Na2S NaHCO3 |
水解 |
ClO-、S2- HCO3- |
pH>7 |
(1)组成盐的弱碱阳离子(M+)能水解显酸性,组成盐的弱酸阴离子(A-)能水解显碱性。
M+ +
H2O  MOH + H+
A- + H2O
MOH + H+
A- + H2O HA + OH-
HA + OH-
(2)盐对应的酸(或碱)越弱,水解程度越大(越弱越水解),溶液碱性(或酸性)越强。
(3)多元弱酸根,正酸根离子比酸式弱酸根离子水解程度大得多,如:CO32-比HCO3-的水解程度大得多,溶液的碱性更强。
(4)弱酸弱碱盐的阴阳离子能双水解,水解程度比单一离子水解程度大,溶液的酸碱性是“谁强显谁性”如:NH4Ac溶液显中性,而(NH4)2S溶液显碱性。
完全双水解的例子:Al3+与CO32-、HCO3-、S2-、HS-、[Al(OH)4]-、ClO-、SiO32-、PO43-、HPO42-等离子发生完全双水解;Fe3+(Fe2+)与CO32-、HCO3-、[Al(OH)4]-、ClO-、SiO32-、PO43-、HPO42-等离子发生完全双水解;NH4+与SiO32-、[Al(OH)4]-等离子发生完全双水解。


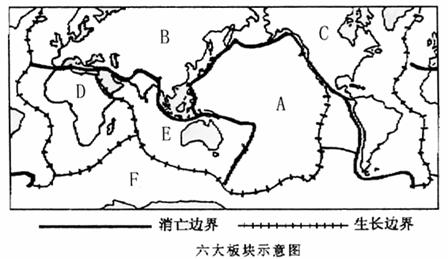 13.读六大板块示意图,完成以下各题:
13.读六大板块示意图,完成以下各题: