摘要:3molCl2通入0.2mol FeBr2溶液中D过量BaCl2溶液与少量Na2SO3溶液相混合少量Ba(NO3)2溶液与过量MgSO4溶液相混合
网址:http://m.1010jiajiao.com/timu_id_445339[举报]
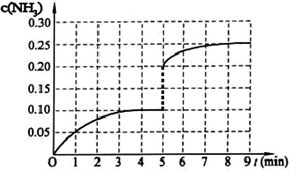
 (2013?广东模拟)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
(2013?广东模拟)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:(1)根据下图,计算从反应开始到平衡时,平均反应速率v(NH3)=
0.025mol/(L?min)
0.025mol/(L?min)
.(2)该反应450℃的平衡常数
>
>
500℃时的平衡常数(填“>”、“<”或“=”).(3)下列描述中能说明上述反应已达平衡的是
BD
BD
.A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
(4)第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡
不
不
移动(填“向正反应方向”、“向逆反应方向”或“不”).(5)第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡
(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.

A、B、C是三种常见短周期元素的单质.常温下D为无色液体,E是一种常见的温室气体.其转化关系如图(反应条件和部分产物略去).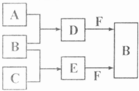 试回答:
试回答:
(1)E的电子式是
 .
.
(2)单质X和B或D均能反应生成黑色磁性固体Y,Y的化学式是
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等.Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18.Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是
(4)取0.3mol F与足量D充分混合后,所得溶液中再通入0.2mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)
(5)E的大量排放会引发很多环境问题.有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用.25℃,101kPa时,该反应的热化学方程式是
查看习题详情和答案>>
 试回答:
试回答:(1)E的电子式是


(2)单质X和B或D均能反应生成黑色磁性固体Y,Y的化学式是
Fe3O4
Fe3O4
.(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等.Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18.Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是
O3+2H++2I-=O2+I2+H2O
O3+2H++2I-=O2+I2+H2O
.(4)取0.3mol F与足量D充分混合后,所得溶液中再通入0.2mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)
c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)
c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)
.(5)E的大量排放会引发很多环境问题.有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用.25℃,101kPa时,该反应的热化学方程式是
CO2(g)+3H2(g)=CH3OH(l)+H2O(1)△H=-130.9kJ/mol
CO2(g)+3H2(g)=CH3OH(l)+H2O(1)△H=-130.9kJ/mol
.(已知甲醇的燃烧热△H=-726.5kJ?mol-1,氢气的燃烧热△H=-285.8kJ?mol-1)一定温度下,向1L密闭容器中通入0.2mol NO和0.1molBr2,保持一定条件发生反应:
2NO(g)+Br2(g)=2NOBr(g)中.Br2的物质的量n(Br2)随时间变化的实验数据如下表:
根据表中数据,下列说法正确的是( )
2NO(g)+Br2(g)=2NOBr(g)中.Br2的物质的量n(Br2)随时间变化的实验数据如下表:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| n(Br2)/mol | 0.080 | 0.075 | 0.072 | 0.070 | 0.070 | 0.070 |
| A、20 min后浓度不再变化,是因为反应已停止 |
| B、10 min内Br2的平均反应速率是0.0025 mol/(L?min) |
| C、25 min~30 min过程中,NO的物质的量浓度逐渐降低 |
| D、20 min时,容器中NO和Br2的物质的量浓度相等 |
在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:
N2(g)+3H2(g)?2NH3(g)△H<0
(1)该反应450℃的平衡常数
(2)下列描述中能说明上述反应已达平衡的是
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为
(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡
查看习题详情和答案>>
N2(g)+3H2(g)?2NH3(g)△H<0
(1)该反应450℃的平衡常数
>
>
500℃时的平衡常数(填“>”、“<”或“=”);(2)下列描述中能说明上述反应已达平衡的是
bd
bd
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为
0.01
0.01
mol/(L?min)(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:
a+
=0.2,b+
=0.6
| c |
| 2 |
| 3c |
| 2 |
a+
=0.2,b+
=0.6
;| c |
| 2 |
| 3c |
| 2 |
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡
正反应方向
正反应方向
移动(填“向正反应方向”“向逆反应方向”或“不”).