题目内容
在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:
N2(g)+3H2(g)?2NH3(g)△H<0
(1)该反应450℃的平衡常数
(2)下列描述中能说明上述反应已达平衡的是
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为
(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡
N2(g)+3H2(g)?2NH3(g)△H<0
(1)该反应450℃的平衡常数
>
>
500℃时的平衡常数(填“>”、“<”或“=”);(2)下列描述中能说明上述反应已达平衡的是
bd
bd
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol计算从反应开始到平衡时,平均反应速率v(N2)为
0.01
0.01
mol/(L?min)(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:
a+
=0.2,b+
=0.6
| c |
| 2 |
| 3c |
| 2 |
a+
=0.2,b+
=0.6
;| c |
| 2 |
| 3c |
| 2 |
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,则平衡
正反应方向
正反应方向
移动(填“向正反应方向”“向逆反应方向”或“不”).分析:(1)对于放热反应,温度越高,平衡常数越小;
(2)反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断;
(3)根据化学反应速率公式v=
来计算反应速率;
(4)根据极限转化的思想结合等效平衡知识来解决;
(5)根据增大反应物浓度化学平衡向着正反应方向进行来回答.
(2)反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断;
(3)根据化学反应速率公式v=
| △c |
| △t |
(4)根据极限转化的思想结合等效平衡知识来解决;
(5)根据增大反应物浓度化学平衡向着正反应方向进行来回答.
解答:解:(1)该反应是放热的,对于放热反应,温度越高,平衡常数越小,所以450℃的平衡常数>500℃时的平衡常数,故答案为:>;
(2)a.化学反应速率之比等于系数之比,当2v正(H2)=3v逆(NH3)才证明平衡,故a错误;
b.容器中气体的平均相对分子量M=
,n对于该反应来说是变化的,当n不变化了,即M不变化了,达到平衡,故b正确;
c.容器中气体的密度ρ=
,密度始终是不随时间而变化的一个定值,故c错误;
d.容器中气体的分子总数不随时间而变化证明各组分浓度保持不变了,故d正确;
故选bd;
(3)第5分钟时达到平衡,测得NH3的物质的量为0.2mol,所以减小的氮气物质的量为0.1mol,v(N2)=
=0.01mol/(L?min),故答案为:0.01;
(4)初始投入量为amolN2、bmolH2、cmolNH3,极限转化为氮气和氢气,相当于投料为:(a+
)mol的氮气和(b+
)mol的氢气,得到与上述相同的平衡,则a+
=0.2,b+
=0.6,故答案为:a+
=0.2,b+
=0.6;
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,相当于增大了反应物的浓度,增大反应物浓度化学平衡向着正反应方向进行,故答案为:正反应方向.
(2)a.化学反应速率之比等于系数之比,当2v正(H2)=3v逆(NH3)才证明平衡,故a错误;
b.容器中气体的平均相对分子量M=
| m |
| n |
c.容器中气体的密度ρ=
| m |
| V |
d.容器中气体的分子总数不随时间而变化证明各组分浓度保持不变了,故d正确;
故选bd;
(3)第5分钟时达到平衡,测得NH3的物质的量为0.2mol,所以减小的氮气物质的量为0.1mol,v(N2)=
| ||
| 5min |
(4)初始投入量为amolN2、bmolH2、cmolNH3,极限转化为氮气和氢气,相当于投料为:(a+
| c |
| 2 |
| 3c |
| 2 |
| c |
| 2 |
| 3c |
| 2 |
| c |
| 2 |
| 3c |
| 2 |
(5)第5分钟末,保持其它条件不变,若继续通入0.2mol的N2和0.6mol的H2,相当于增大了反应物的浓度,增大反应物浓度化学平衡向着正反应方向进行,故答案为:正反应方向.
点评:本题涉及化学反应速率的计算、平衡状态的判断以及化学平衡的有关计算知识,可以根据所学知识来回答,难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
(12分))氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。(1)上图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式 。
(2)已知:N2(g)+ O2(g)=2 NO(g) △H = +180 kJ • mol-1
2NO(g)+2 CO(g)= N2(g) + 2 CO2(g) △H = - 746 kJ • mol-1
则反应CO(g) +![]() O2(g) = CO2(g)的△H = kJ• mol-1
O2(g) = CO2(g)的△H = kJ• mol-1
(3)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g)![]() 2NH3(g) △H <0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为 ,该反应的平衡常数表达式K = 。
2NH3(g) △H <0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为 ,该反应的平衡常数表达式K = 。
(4) 在固定体积的密闭容器中,1.0×103 kPa时反应 N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H<0 的平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
①K1 K2(填写“>”、“=”或“<”)
②下列各项能说明上述合成氨反应一定达到平衡状态的是 (填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.NH3的浓度保持不变
c.容器内压强保持不变 d.混合气体的密度保持不变
 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
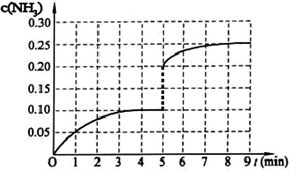
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义. (2013?广东模拟)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
(2013?广东模拟)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: