摘要:化学反应速率的典型实验 P20实验2-1锌与不同浓度硫酸的反应 P22实验2-2 过氧化氢分解 (催化剂是MnO2.FeCl3.CuSO4) P25探究 不同浓度的KMnO4与H2C2O4反应速率,唾液.H2SO4溶液对淀粉水解的催化作用
网址:http://m.1010jiajiao.com/timu_id_437501[举报]
甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素.其设计的实验方案如下,请你帮他填写完整,并做出评价.
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
【评价】甲同学设计的实验方案的合理性是
A.非常合理B.部分合理C.完全不合理
【补充和完善】上一项若填A,则此项不用再作答,若填B或C,则完成实验还需要的试剂是
(2)探究影响化学反应速率的因素
甲同学所得实验依据和结论有明显问题,问题是
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性.画出实验装置图,标出正负极、电子流动方向,写出电极反应式.
装置图

电极反应式
查看习题详情和答案>>
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
| 实验步骤 | 实验现象 | 实验结论及离子方程式 |
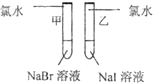 |
甲 溶液由无色变为橙色 溶液由无色变为橙色 乙 溶液由无色变为黄色 溶液由无色变为黄色 |
离子方程式 甲: 2Br-+Cl2═Br2+2Cl- 2Br-+Cl2═Br2+2Cl- 乙: 2I-+Cl2═2Cl-+I2 2I-+Cl2═2Cl-+I2 结论:卤素单质的氧化强到弱的顺序为Cl2>Br2>I2 |
B
B
(填序号)A.非常合理B.部分合理C.完全不合理
【补充和完善】上一项若填A,则此项不用再作答,若填B或C,则完成实验还需要的试剂是
溴水
溴水
.(2)探究影响化学反应速率的因素
| 实验步骤 | 实验现象 | 实验依据和结论 |
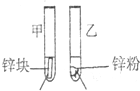 3mL1mol/L 3mL3mol/L 盐酸 盐酸 (金属质量相同,盐酸均过量) |
均有气体生成,锌粉先消失,锌块后消失 | 因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快. |
锌粉的表面积大,也能加快反应速率
锌粉的表面积大,也能加快反应速率
.(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性.画出实验装置图,标出正负极、电子流动方向,写出电极反应式.
装置图

电极反应式
负极:Fe-2e-═Fe2+
负极:Fe-2e-═Fe2+
正极:2H++2e-═H2↑
正极:2H++2e-═H2↑
.物质的浓度差异可导致物质的性质发生改变,不同浓度的物质在发生化学反应时其反应速率也会发生改变.
(1)浓硫酸具有:①强氧化性;②吸水性;③脱水性.以下过程主要表现浓硫酸的那些性质?请将答案填在横线上.
a.纸张、木条等遇浓硫酸会慢慢变黑;
b.浓硫酸可用于干燥H2、O2、SO2等气体;
c.常温下,铁或铝在浓硫酸中钝化;
(2)某学生进行了“浓度影响化学反应速率”的探究实验,原始数据记录如下:
①上述反应的方程式为:Zn+H2SO4=ZnSO4+H2↑,该反应既属于氧化还原反应,又属于
②比较两组数据可知:硫酸的浓度越大,化学反应速率
查看习题详情和答案>>
(1)浓硫酸具有:①强氧化性;②吸水性;③脱水性.以下过程主要表现浓硫酸的那些性质?请将答案填在横线上.
a.纸张、木条等遇浓硫酸会慢慢变黑;
③
③
(填写序号,下同).b.浓硫酸可用于干燥H2、O2、SO2等气体;
②
②
.c.常温下,铁或铝在浓硫酸中钝化;
①
①
.(2)某学生进行了“浓度影响化学反应速率”的探究实验,原始数据记录如下:
| Zn的质量 | H2SO4的浓度 | 收集20mL H2所需的时间 | |
| ① | 10g(锌粉) | 0.1mol/L | 125s |
| ② | 10g(锌粉) | 0.2mol/L | 62s |
置换反应
置换反应
反应(填四大基本反应类型名称).②比较两组数据可知:硫酸的浓度越大,化学反应速率
越快
越快
(填“越快”、“越慢”或“不变”).某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。
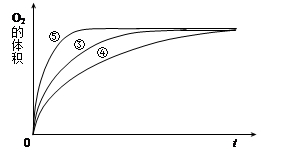
分析上图能够得出的实验结论是______________________________________。 查看习题详情和答案>>
某学生做浓度对化学反应速率的影响实验时,将3支试管编号为①②③,并按下表中的物质的量进行实验,记录的时间数据是16s、28s、33s。请将3个时间数据填入下表的适当位置,并写出实验结论。
| 试管编号 | 加3%Na2S2O3溶液/ml | 加H2O/ml | 加H2SO4(1:5)/滴 | 出现浑浊所用时间/s |
| ① | 3[ | 3 | 5 | a |
| ② | 4 | 2 | 5[] | b |
| ③ | 5 | 1 | 5 | c |
(2)实验结论:
(3)写出反应的化学方程式:
 [来源:
查看习题详情和答案>>
[来源:
查看习题详情和答案>>
常温下按照如下方案完成实验。
|
实验编号 |
反应物 |
催化剂 |
|
① |
10mL2% H2O2溶液 |
无 |
|
② |
10mL5% H2O2溶液 |
无 |
|
③ |
10mL5% H2O2溶液 |
1mL0.1mol·L-1FeCl3溶液 |
|
④ |
10mL5% H2O2溶液+少量HCl溶液 |
1mL0.1mol·L-1FeCl3溶液 |
|
⑤ |
10mL5% H2O2溶液+少量NaOH溶液 |
1mL0.1mol·L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_____________________________________。
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。

分析上图能够得出的实验结论是______________________________________。
查看习题详情和答案>>