题目内容
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(2)实验①和②的目的是____________________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是____________________。
(3)写出实验③的化学反应方程式 。
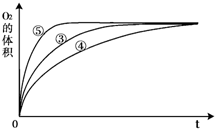
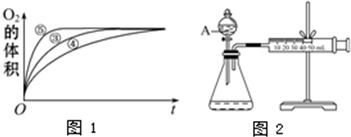
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。
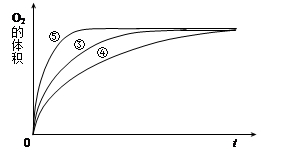
分析上图能够得出的实验结论是______________________________________。
(8分)(1)降低了活化能(2)探究浓度对反应速率的影响
向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中)
(3)2H2O2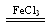 O2↑+2H2O
O2↑+2H2O
(4)碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率
解析试题分析:(1)催化剂能加快化学反应速率的原因是催化剂可用降低反应的活化能,从而加快应速率。
(2)实验①和②中只有双氧水的浓度不同,所以的目的是探究浓度对反应速率的影响。要加快反应速率则可用通过加入催化剂或升高温度,即向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中)。
(3)双氧水在催化剂的作用下分解生成氧气和水,即2H2O2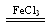 O2↑+2H2O。
O2↑+2H2O。
(4)实验③、④、⑤中不同之处在于溶液的酸碱性不同,所以根据图像可知碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率。
考点:考查外界条件对双氧水分解反应速率的实验探究
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。

练习册系列答案
相关题目
H2O2是实验室常用的一种化学试剂.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)实验①和②的目的是 ,
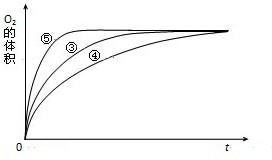
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析下图能够得出的结论是 .
(3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是 .
(4)H2O2能氧化H2SO4 酸化的FeSO4,离子方程式为 ;
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析下图能够得出的结论是
(3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是
(4)H2O2能氧化H2SO4 酸化的FeSO4,离子方程式为

某实验小组以H2O2分解为例,研究浓度、催化剂对反应速率的影响.在常温下按照如下方案完成实验.实验②的反应物应( )
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 无 | |
| ③ | 10mL 5% H2O2溶液 | MnO2 固体 |
| A、5mL 2% H2O2溶液 |
| B、10mL 5% H2O2溶液 |
| C、10mL 2% H2O2溶液 |
| D、5mL 10% H2O2溶液 |
H2O2是实验室常用的一种化学试剂.
I.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)实验①和②的目的是 ,实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是 .
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析图能1够得出的实验结论是 .

Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
(1)实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,则实验中需要测量的数据是 .
(2)加入0.1g mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示.解释反应速率变化的原因 ,计算H2O2的初始物质的量浓度 .(保留两位有效数字)
I.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析图能1够得出的实验结论是

Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
(1)实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,则实验中需要测量的数据是
(2)加入0.1g mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示.解释反应速率变化的原因
 (2011?顺德区模拟)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(2011?顺德区模拟)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验. O2↑+2H2O
O2↑+2H2O