摘要:㈠半径比较1. 原子半径的大小取决于两个因素:一是电子的能层数.另一个是 .同主族元素随着原子序数的增加.电子能层数逐渐增多.原子半径逐渐 .同周期元素电子能层数相同.从左往右 逐渐增大.原子半径逐渐 .
网址:http://m.1010jiajiao.com/timu_id_4219587[举报]
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.
请回答:
(1)画出元素⑨的原子结构示意图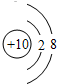
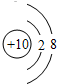 .
.
(2)九种元素中非金属性最强的是
(3)①、②两种元素原子半径比较:①
(4)⑦、⑧两种元素组成的氢化物的热稳定性比较:⑦
(5)元素⑤对应的氢化物的化学式是
(6)①、⑥两元素形成的化合物的电子式为
 ,该化合物是由
,该化合物是由
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑦ | ⑨ | |||
| 3 | ① | ② | ③ | ⑧ |
(1)画出元素⑨的原子结构示意图
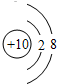
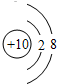
(2)九种元素中非金属性最强的是
F
F
(填元素符号).(3)①、②两种元素原子半径比较:①
>
>
②(填“<”或“>”).在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是NaOH
NaOH
(填化学式).(4)⑦、⑧两种元素组成的氢化物的热稳定性比较:⑦
>
>
⑧(填“<”或“>”).(5)元素⑤对应的氢化物的化学式是
NH3
NH3
,其水溶液的pH>
>
7(填“<”或“>”).④、⑤两种元素对应的最高价含氧酸的酸性强的是HNO3
HNO3
(填化学式).(6)①、⑥两元素形成的化合物的电子式为


离子
离子
(填“共价键”“离子键”)键形成的.①②③④⑤五种元素,在元素周期表中的位置如图所示.回答下列问题
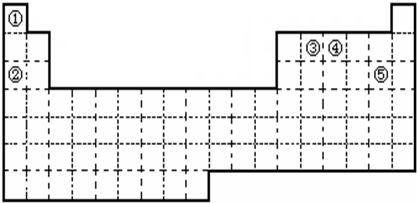
(1)①②③④⑤五种元素中,金属性最强的元素是
(2)元素②的最高价氧化物对应的水化物的电子式为
 ,试比较②和③原子半径的大小②
,试比较②和③原子半径的大小②
(3)画出元素④的原子结构示意图
 ,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)
,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)
(4)写出元素⑤在周期表中的位置
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外L层电子数是M层电子数的4倍.
①甲、乙元素分别为
②写出②的最高价氧化物对应的水化物与甲的最高价氧化物反应的离子方程式
(6)已知破坏1mol N≡N键、H-H键、N-H键分别需要吸收的能量为946kJ、436kJ、391kJ.则1molN2完全反应转化为NH3共
查看习题详情和答案>>

(1)①②③④⑤五种元素中,金属性最强的元素是
钠
钠
(写元素名称),该元素的单质在空气中燃烧的化学方程式为2Na+O2
Na2O2
| ||
2Na+O2
Na2O2
.
| ||
(2)元素②的最高价氧化物对应的水化物的电子式为


>
>
③(填“>”或“<”)(3)画出元素④的原子结构示意图


HNO3
HNO3
.(4)写出元素⑤在周期表中的位置
第三周期ⅦA 族
第三周期ⅦA 族
,以海水中含量最大的物质为原料可以生产⑤的单质,同时还可以得到另外两种重的工业原料,该反应的化学方程式为2NaCl+2H2O
Cl2↑+H2↑+2NaOH
| ||
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
.
| ||
(5)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外L层电子数是M层电子数的4倍.
①甲、乙元素分别为
铝
铝
、镁
镁
写元素名称)②写出②的最高价氧化物对应的水化物与甲的最高价氧化物反应的离子方程式
2NaOH+Al2O3=2NaAlO2+H2O
2NaOH+Al2O3=2NaAlO2+H2O
(6)已知破坏1mol N≡N键、H-H键、N-H键分别需要吸收的能量为946kJ、436kJ、391kJ.则1molN2完全反应转化为NH3共
放出
放出
(填“吸收”或“放出”)能量92
92
kJ.下表列出了A~R 9种元素在周期表中的位置
用元素符号填写下空:
(1)这9中元素中金属性最强的是
(2)化学性质最不活泼的元素是
(3)G的最高价含氧酸的化学式是
(4)E的最简单氢化物的化学式
(5)A在F中燃烧得到产物的化学式
(6)C与D的原子半径比较:R(C)
查看习题详情和答案>>
| 周期族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(1)这9中元素中金属性最强的是
K
K
;(2)化学性质最不活泼的元素是
Ar
Ar
;(3)G的最高价含氧酸的化学式是
HClO4
HClO4
;(4)E的最简单氢化物的化学式
CH4
CH4
;(5)A在F中燃烧得到产物的化学式
Na2O2
Na2O2
;(6)C与D的原子半径比较:R(C)
>
>
R(D)(填“>”或“<”)元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.
请回答:
(1)画出元素⑨的原子结构示意图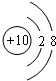
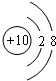 .
.
(2)九种元素中非金属性最强的是
(3)①②两种元素原子半径比较:①
(4)⑦⑧两种元素组成的氢化物的热稳定性比较:⑦
(5)元素⑤对应的氢化物的化学式是
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑦ | ⑨ | |||
| 3 | ① | ② | ③ | ⑧ |
(1)画出元素⑨的原子结构示意图
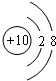
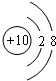
(2)九种元素中非金属性最强的是
F
F
(填元素符号).(3)①②两种元素原子半径比较:①
>
>
②(填“<”或“>”).在①②③三种元素的氧化物对应的水化物中,碱性最强的是NaOH
NaOH
(填化学式).(4)⑦⑧两种元素组成的氢化物的热稳定性比较:⑦
>
>
⑧(填“<”或“>”).(5)元素⑤对应的氢化物的化学式是
NH3
NH3
,其水溶液的pH>
>
7(填“<”或“>”).④⑤两种元素对应的最高价含氧酸的酸性强的是HNO3
HNO3
(填化学式).A、B、C、D、E、F、G全为短周期元素,它们在中学常见化合物中显示的部分化合价及原子、离子半径从大到小的序号如下:(注:半径按①、②、③…的顺序依次减小)
(1)用电子式表示BA2的形成过程
 .
.
(2)写出F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物反应的离子方程式
(3)请设计实验比较B、F的活动性强弱.
查看习题详情和答案>>
| 元素 性质 |
A | B | C | D | E | F | G |
| 化合价 | +1、+5、+7 | 只有+2 | +4 | -3、+2、+4、+5 | 只有-1 | 只有+3 | 只有+1 |
| 原子半径 | ⑤ | ② | ④ | ⑥ | ⑦ | ③ | ① |
| 离子半径 | ① | ⑤ | 无离子 | ② | ③ | ⑥ | ④ |


(2)写出F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物反应的离子方程式
Al(OH)3+OH-═AlO2-+2H2O.
Al(OH)3+OH-═AlO2-+2H2O.
.(3)请设计实验比较B、F的活动性强弱.
| 元素 | 实验设计 | 现象 | 结论 |
| B | 活动性:B F (填“>”、“<”或“=”) | ||
| F |