摘要:接入气球后改进的集气.洗气装置.具有下列优点:①可形成容积可变性密闭系统.具有一定的缓冲功能.②作尾气处理装置.用气球收集多余的气体.避免刺激性.有毒气体的逸漏.例如.制备Cl2时.用图2装置收集多余Cl2.可大大降低实验室内的Cl2浓度.给学生创造良好的实验环境.减弱有毒气体对人体的危害.③用气球收集多余的气体.变废为宝.例如.制备HCl气体时.用气球收集余气.悬挂于室内.可备后用.既可美化实验室.减少有毒气体对环境的污染.又可取之即用.节省药品.(二)气体爆鸣实验中的妙用将集满H2的气球.或悬于铁架台上.或握于手上.或置于桌上.让燃着的火柴靠近气球.气球立即发生粉碎性爆炸.同样.气球可用于CO.CH4等组成的爆鸣气的爆鸣实验.操作简便.安全.(三)在气体溶解性演示实验中的妙用
网址:http://m.1010jiajiao.com/timu_id_412497[举报]
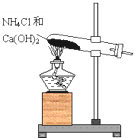 实验室通常用如图所示的装置来制取氨气.回答下列问题:
实验室通常用如图所示的装置来制取氨气.回答下列问题:(1)制取氨气时的化学反应方程式为:
(2)收集氨气时必须使用干燥的集气装置的原因是
(3)加热后将蘸有浓盐酸的玻璃棒靠近导管口,产生的现象是:
某学校研究性学习小组的三位同学,欲用浓硝酸来测定其铜银合金中铜的质量分数。已知:在反应过程中,随着浓硝酸浓度的降低,还原产物中还会有NO生成。请针对这三位同学的设计,完成下列问题:

(1)甲同学取合金样品14.0 g加入A中,然后将装置A、B相连,并向A中加入13.0 mol·L-1的硝酸25.0 mL充分反应后测得生成气体的体积为2.24 L(标准状况下),及反应后容器A中溶液H+浓度为1.0 mol·L-1(假设反应后溶液体积不变)。利用以上数据,你认为甲同学能得到合金中铜的质量分数吗?如果能,请写出计算过程及结果;如果不能,请简述理由。
(2)乙同学将装置A、C相连,向A中加入w g合金样品和足量浓硝酸充分反应,将生成的气体简单作了吸收处理后,便向反应后的A溶液中加入一种常见试剂,充分反应后,再经过简单的实验操作就达到了目的。请你简述他的实验思路。
(3)丙同学将装置A、D相连,向A中加入一定质量的合金样品和足量浓硝酸,充分反应后用排水集气法测定了生成气体的体积,也达到了实验目的。
①D中发生反应的化学方程式:______________________________________________。
②假设已知合金中Cu、Ag的总物质的量为a mol,水洗后气体的体积是b L(标准状况下),则合金中Cu的物质的量是___________。(结果不必简化)
查看习题详情和答案>>用铝箔包裹0.1 mol金属钠,用针扎出一些小孔,放入水中,完全反应后用排水集气法收集产生的气体,则收集到的气体为(标准状况)
[ ]
A.O2和H2的混合气体
B.1.12 L H2
C.大于1.12 L H2
D.小于1.12 L H2
查看习题详情和答案>>
B.1.12 L H2
C.大于1.12 L H2
D.小于1.12 L H2
(1)野外焊接钢轨的铝热反应
(2)用蘸有浓盐酸的玻璃棒靠近装有氨气的集气瓶口
(3)金属铝与氢氧化钠溶液反应
(4)铁粉与水蒸气在高温条件下反应
(5)过氧化钠与水反应
(6)铁在氯气中燃烧
(7)红棕色的二氧化氮气体与水反应
(8)铜与稀硝酸反应
(9)实验室贮存氢氧化钠溶液的试剂瓶用橡胶塞的原理
(10)氯气的尾气处理原理
查看习题详情和答案>>
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
| ||
(2)用蘸有浓盐酸的玻璃棒靠近装有氨气的集气瓶口
HCl+NH3=NH4Cl
HCl+NH3=NH4Cl
(3)金属铝与氢氧化钠溶液反应
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(4)铁粉与水蒸气在高温条件下反应
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
| ||
(5)过氧化钠与水反应
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
(6)铁在氯气中燃烧
2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
| ||
(7)红棕色的二氧化氮气体与水反应
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
(8)铜与稀硝酸反应
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(9)实验室贮存氢氧化钠溶液的试剂瓶用橡胶塞的原理
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
(10)氯气的尾气处理原理
Cl2+2NaOH=NaCl+NaClO+H2O
Cl2+2NaOH=NaCl+NaClO+H2O
.