摘要:4.钠和氧气的反应(1)实验过程:①②③④⑤⑥⑦
网址:http://m.1010jiajiao.com/timu_id_405462[举报]
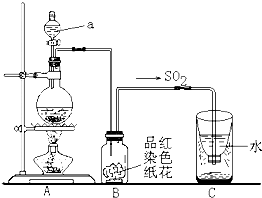 实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气.
实验制取乙烯时,应将乙醇和浓硫酸快速加热到170℃,在140℃时会生成乙醚,温度过高会使部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气.(1)分别写出乙醇跟浓H2SO4反应生成①脱水生成CH2=CH2;②分子间脱水生成CH3CH2-O-CH2CH3;③SO2、CO2、水蒸气的化学方程式:①
CH3CH2OH
CH2═CH2↑+H2O
| 浓硫酸 |
| 170℃ |
CH3CH2OH
CH2═CH2↑+H2O
;②| 浓硫酸 |
| 170℃ |
2CH3CH2OH
CH3CH2OCH2CH3+H2O
| 浓硫酸 |
| 140℃ |
2CH3CH2OH
CH3CH2OCH2CH3+H2O
;③| 浓硫酸 |
| 140℃ |
CH3CH2OH+H2SO4
H2O+SO2↑+CO2↑
| 高温 |
CH3CH2OH+H2SO4
H2O+SO2↑+CO2↑
;| 高温 |
(2)二氧化硫是大气污染物之一,空气中的二氧化硫随雨水下降形成酸雨.如图实验装置,对酸雨的形成进行模拟并验证二氧化硫的部分性质,请回答:
①指出图中仪器a的名称:
分液漏斗
分液漏斗
.②B装置中淡红色纸花的颜色逐渐变褪去,说明SO2有
漂白
漂白
性.③反应结束后取出C装置中少量液体,滴加紫色石蕊试液后变
红
红
色.④实验完毕后.为了使多余的二氧化硫被充分吸收,C装置应如何改进?(用文字说明)
向C中加入过量的氢氧化钠溶液,震荡后静置
向C中加入过量的氢氧化钠溶液,震荡后静置
.实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案: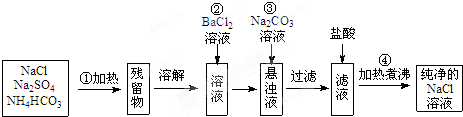
如果此方案正确,那么:
(1)操作①中碳酸氢铵受热(100℃以上)可分解生成氨气、水和二氧化碳的混合气,该混合气的平均摩尔质量为
(2)操作②为什么不能改为加硝酸钡溶液?
(3)操作③的目的是
(4)操作④的目的是
查看习题详情和答案>>

如果此方案正确,那么:
(1)操作①中碳酸氢铵受热(100℃以上)可分解生成氨气、水和二氧化碳的混合气,该混合气的平均摩尔质量为
26.3g/mol
26.3g/mol
.(数值保留到小数点后一位)(2)操作②为什么不能改为加硝酸钡溶液?
改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,以后操作中无法除去
改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,以后操作中无法除去
.(3)操作③的目的是
发生反应Na2CO3+BaCl2═BaCO3↓+2NaCl,除去过量的Ba2+
发生反应Na2CO3+BaCl2═BaCO3↓+2NaCl,除去过量的Ba2+
(结合化学方程式回答).(4)操作④的目的是
除去滤液中溶解的CO2和多余的盐酸
除去滤液中溶解的CO2和多余的盐酸
.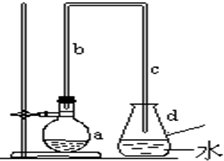 实验室用如图装置制取少量溴苯.
实验室用如图装置制取少量溴苯.(1)在烧瓶a中装的试剂是
苯
苯
、液溴
液溴
和铁
铁
.导管b的作用有两个:一是导气
导气
,二是兼起冷凝
冷凝
的作用.(2)反应过程中在导管c的下口附近可以观察到有
白雾
白雾
出现,这是由于反应生成的HBr
HBr
遇水蒸气而形成的.(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液有
浅黄色沉淀生成
浅黄色沉淀生成
生成,写出离子方程式:Ag++Br-=AgBr↓
Ag++Br-=AgBr↓
.(4)反应完毕后,将烧瓶中a的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有
褐
褐
色不溶于水的液体.这是因为溴苯中溶解了溴单质
溶解了溴单质
.纯溴苯是无
无
色液
液
体,除去杂质所需的试剂是氢氧化钠溶液
氢氧化钠溶液
,用分液
分液
方法分离.(5)写出烧瓶a中发生反应的化学方程式:
C6H6+Br2
C6H5Br+HBr
| Fe |
C6H6+Br2
C6H5Br+HBr
.| Fe |
实验室里可用图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质. ?
?
图中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液?
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
图2中符合该晶体溶解度曲线的是
(3)本实验中制取次氯酸钠的离子方程式是
查看习题详情和答案>>
 ?
?图中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过
分液漏斗
分液漏斗
(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B
B
(填写下列编号字母)的净化装置.A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液?
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
碱溶液(或反应物)的浓度不同,反应温度不同?
碱溶液(或反应物)的浓度不同,反应温度不同?
反应完毕经冷却后,②的试管中有大量晶体析出.图2中符合该晶体溶解度曲线的是
M
M
(填写编号字母);冷却后从②的试管中分离出该晶体的方法是过滤
过滤
(填写实验操作名称).(3)本实验中制取次氯酸钠的离子方程式是
Cl2+2OH-═ClO-+Cl-+H2O
Cl2+2OH-═ClO-+Cl-+H2O
,实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | |
| 然后溶液从无色逐渐变为 黄绿 黄绿 色 |
 实验室制乙烯通常采用乙醇与浓硫酸(体积比为1:3)混合加热到170℃制得,反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过如图实验装置.(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用.)
实验室制乙烯通常采用乙醇与浓硫酸(体积比为1:3)混合加热到170℃制得,反应过程中乙醇常被炭化,溶液中有黑色物质出现,随着反应进行炭化现象越来越严重,同时制得的乙烯气体中通常会含有CO2、SO2等气体,为确认混合气体中含有乙烯和二氧化硫,可让混合气体依次通过如图实验装置.(可供选择的试剂:品红溶液、氢氧化钠溶液、溴水、酸性高锰酸钾溶液、浓硫酸,试剂可重复使用.)A.①②中盛放的试剂分别为①
品红
品红
; ②NaOH溶液
NaOH溶液
;(填试剂名称)B.能说明二氧化硫气体存在的现象是
装置①中品红褪色
装置①中品红褪色
.C.能确认含有乙烯的现象是
装置③中品红不褪色,装置④中溶液褪色
装置③中品红不褪色,装置④中溶液褪色
.