摘要:答题时书写要规范.要用源于课本的学科语言.8个式子(化学式.电子式.结构式.结构简式.实验式.化学方程式.离子方程式.热化学方程式)一个图.可逆符号.气体符号.沉淀符号的使用.总之.解无机推断题的基本思想是鼓励学生在积累了丰富的知识之后大胆尝试.大胆猜想.要相信这个时候异想天开,往往能够茅塞顿开;胆大妄为,往往就会大有作为.
网址:http://m.1010jiajiao.com/timu_id_403708[举报]
实验室要用12mol/L的浓盐酸配制1.0mol/L的稀盐酸91mL.
(1)要配制上述溶液,需用
(2)配制过程中,除(1)中所选仪器、以及烧杯、玻璃棒、胶头滴管外,还需用到的仪器有
(3)A、B是配制溶液时可能用到的二种仪器的一部分,请根据提供的情景按要求回答问题.
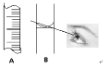
①写二种仪器的名称A
②若按B中视线观察液面,则还需要继续进行的操作是
此操作完毕时,配制溶液的浓度
查看习题详情和答案>>
(1)要配制上述溶液,需用
10mL量筒
10mL量筒
量取12mol/L的浓盐酸8.3
8.3
mL.(2)配制过程中,除(1)中所选仪器、以及烧杯、玻璃棒、胶头滴管外,还需用到的仪器有
100mL容量瓶
100mL容量瓶
.(3)A、B是配制溶液时可能用到的二种仪器的一部分,请根据提供的情景按要求回答问题.

①写二种仪器的名称A
量筒
量筒
;B容量瓶
容量瓶
.②若按B中视线观察液面,则还需要继续进行的操作是
用胶头滴管滴加蒸馏水直到与容量瓶刻线相切
用胶头滴管滴加蒸馏水直到与容量瓶刻线相切
;此操作完毕时,配制溶液的浓度
偏低
偏低
(填偏高、偏低、相符).分别取40mL的0 50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
(2)为什么中和热测定中要用稍过量的碱(或酸):
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/(g?℃).为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=
(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
查看习题详情和答案>>
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、
环形玻璃搅拌棒
环形玻璃搅拌棒
、量筒
量筒
.(2)为什么中和热测定中要用稍过量的碱(或酸):
为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热
为了保证酸(或碱)能够完全被中和或通过测量值求算的是反应生成1mol水时的反应热即中和热
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4 18J/(g?℃).为了计算中和热,某学生实验记录数据如下:

依据该学生的实验数据计算,该实验测得的中和热△H=
-50.2KJ/mol
-50.2KJ/mol
; (结果保留一位小数)(4)上述实验数值结果与中和热的理论值57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)
abd
abd
.a.实验装置保温、隔热效果差 b.量取盐酸与氢氧化钠溶液时仰视读数c.分多次把Na0H溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度.
(2011?南京一模)乙酰水杨酸即阿司匹林,可通过水杨酸与乙酸酐反应制得:

乙酰水杨酸能与碳酸铺反直生成水溶性盐,而副产物聚合物不溶于碳酸钠溶液.
制取乙酰水杨酸的定验步骤如下
(1)投料.在125ml的锥形瓶中依次加2g水杨酸,5ml 乙酸酐,5滴浓硫酸,小心旋转锥形瓶使水杨酸全部溶解后,加热5~1Omin,控带尝试在85~95℃.
①试剂添加时如果先加水杨酸鞠和浓硫酸,产率会降低,原因是
②最合适的加热方法是
(2)粗产品结晶.取出锥形瓶,边摇边滴加1ml冷水,然后快速加入50ml 冷水,立即进入冰浴冷却.待晶体完全析出后用布氏漏斗抽滤,用少量冰水分两次洗涤稚形瓶后,再洗涤晶体,抽干.洗涤晶体要用少量冰水的原因是
(3)粗产品提纯.将粗产品转移到150ml烧杯中.在搅拌下慢慢加入适量
(4)纯度检验.检验粗产品中是否含有水杨酸,可取少许产品加入盛有5mL水的试管中,加入 1~2滴
查看习题详情和答案>>

乙酰水杨酸能与碳酸铺反直生成水溶性盐,而副产物聚合物不溶于碳酸钠溶液.
| 药品名称 | 相对分子质量 | 熔点(℃) | 沸点(℃) | 溶解度(g/100mL水) |
| 水杨酸 | 138.12 | 159 | 211(2.66kPa) | 微溶于冷水,易溶于热水 |
| 乙酸酐 | 102.09 | -73 | 139 | 在水中逐渐分解 |
| 乙酰水杨酸 | 180.16 | 135~138 | 微溶于水 |
(1)投料.在125ml的锥形瓶中依次加2g水杨酸,5ml 乙酸酐,5滴浓硫酸,小心旋转锥形瓶使水杨酸全部溶解后,加热5~1Omin,控带尝试在85~95℃.
①试剂添加时如果先加水杨酸鞠和浓硫酸,产率会降低,原因是
水杨酸会被氧化
水杨酸会被氧化
.②最合适的加热方法是
水浴加热
水浴加热
.(2)粗产品结晶.取出锥形瓶,边摇边滴加1ml冷水,然后快速加入50ml 冷水,立即进入冰浴冷却.待晶体完全析出后用布氏漏斗抽滤,用少量冰水分两次洗涤稚形瓶后,再洗涤晶体,抽干.洗涤晶体要用少量冰水的原因是
减少晶体的溶解
减少晶体的溶解
.(3)粗产品提纯.将粗产品转移到150ml烧杯中.在搅拌下慢慢加入适量
饱和碳酸钠溶液
饱和碳酸钠溶液
,加完后继续搅拌几分钟,直到无二氧化碳气体产生
无二氧化碳气体产生
为止.抽滤,副产物聚合物被滤出,用5~10mL水冲洗漏斗,合并滤液,倒入预先盛有4-5ml.浓盐酸和l0ml水配成溶液的烧杯中,搅拌均匀,即有乙酰水杨酸沉淀析出.(4)纯度检验.检验粗产品中是否含有水杨酸,可取少许产品加入盛有5mL水的试管中,加入 1~2滴
三氯化铁或FeCl3
三氯化铁或FeCl3
溶液.观察有无颜色反应.