摘要:25. 2H+ + 2e = H2 ↑ 4 (3)Zn片上有较多气泡.石墨上有少量气泡 [或能够与对比说明]
网址:http://m.1010jiajiao.com/timu_id_393221[举报]
 (1)写出图①中电解池阴阳两极的电极反应式和该电解池的总反应式:
(1)写出图①中电解池阴阳两极的电极反应式和该电解池的总反应式:阴极:
Cu2++2e-=Cu
Cu2++2e-=Cu
;阳极:
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
;电解池总反应式:
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
.
| ||
(2)写出图②中原电池正负两极的电极反应式和该原电池的总反应式:
正极:
2H++2e-=H2↑
2H++2e-=H2↑
;负极:
Zn-2e-=Zn2+
Zn-2e-=Zn2+
;原电池总反应式:
Zn+2HCl=ZnCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
.(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上

(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过.图乙、图丙是一个将
(3)从上述现象中可以归纳出构成原电池的一些条件是
查看习题详情和答案>>
没有
没有
(填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上有
有
(填“有”或“没有”)气泡产生.
(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过.图乙、图丙是一个将
化学
化学
能转化为电
电
能的装置,人们把它叫做原电池.(3)从上述现象中可以归纳出构成原电池的一些条件是
两电极要插入电解质溶液,并用导线连接形成回路
两电极要插入电解质溶液,并用导线连接形成回路
,有关的电极反应式:锌片Zn-2e-=Zn2+
Zn-2e-=Zn2+
;铜片2H++2e-=H2↑
2H++2e-=H2↑
. 一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu→Cu2++2e-,还原反应式:2Fe3++2e-→2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu→Cu2++2e-,还原反应式:2Fe3++2e-→2Fe2+.并由此实现了化学能与电能的相互转化.据此,回答下列问题:(1)将反应Zn+2H+═Zn2++H2↑拆写为两个“半反应式”:其中,氧化反应式为:
Zn=Zn2++2e-
Zn=Zn2++2e-
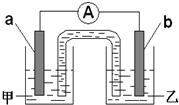
.(2)由题(1)反应,设计成原电池如图所示:若电极a为Zn,电极b可选择材料:
铜
铜
(只填一种);电解质溶液甲是ZnSO4
ZnSO4
;电极b处的电极反应式:2H++2e-=H2↑
2H++2e-=H2↑
.(3)由反应2H2+O2
| ||
2H2-4e-=4H+
2H2-4e-=4H+
,正极O2+4H++4e-=2H2O
O2+4H++4e-=2H2O
.(4)以惰性材料为电极,电解100mL pH=6的硫酸铜溶液,当电解池内溶液的pH为1时,电极上析出的铜的质量为
0.32g
0.32g
(忽略电解前后溶液体积的变化).Ⅰ:元素的金属活动性递变规律是元素周期表学习的重要内容之一.某校研究性学习小组查阅课外资料,看到第IVA族的三种金属锗、锡、铅的性质:“锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅,请解释发生上述变化的原因是
Ⅱ:另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在右侧方框内画出原电池装置图.
并写出正极的反应现象及电极反应式.
现象
(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序.你的设计方法是
查看习题详情和答案>>
铅的活动性比锗和锡都强,易被空气中的氧气氧化
铅的活动性比锗和锡都强,易被空气中的氧气氧化
.Ⅱ:另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在右侧方框内画出原电池装置图.
并写出正极的反应现象及电极反应式.
现象
表面有气泡产生
表面有气泡产生
;电极反应式2H++2e-=H2↑
2H++2e-=H2↑
.(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序.你的设计方法是
先用氧化铜与稀硫酸反应生成硫酸铜,再将铁片插入硫酸铜溶液中置换出铜
先用氧化铜与稀硫酸反应生成硫酸铜,再将铁片插入硫酸铜溶液中置换出铜
.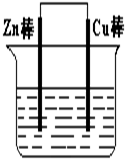 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如下图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如下图所示装置.试回答下列问题: