摘要: Br2 (1)观察待检气体的颜色.如果呈红棕色.并将此气体通入水中.如果此气体水溶液的颜色呈黄色.则证明待检气体是Br2. (2)将待检气体用冰水冷却.如果转化为红棕色的液体.则待检气体为Br2. (3)将待检的红棕色气体通入AgNO3溶液中.如果出现浅黄色的沉淀.则证明待检气体是Br2.
网址:http://m.1010jiajiao.com/timu_id_3832534[举报]
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:
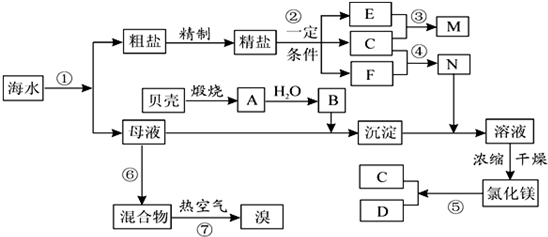
请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N
(2)写出反应②的化学方程式
(3)写出反应③的离子方程式:
Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因:
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有
(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?
查看习题详情和答案>>

请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N
HCl
HCl
、B石灰乳
石灰乳
.(2)写出反应②的化学方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
(3)写出反应③的离子方程式:
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
,Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为
AD
AD
.A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是
C
C
.A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因:
3Mg+N2
Mg3N2
| ||
3Mg+N2
Mg3N2
.
| ||
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是
CD
CD
.A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有
挥发
挥发
性.(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?
乙
乙
(填“甲”或“乙”),理由是若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2
若先提取镁,海水中会残留大量Ca(OH)2,再用Cl2提取溴时会消耗大量Cl2
.海水资源的利用具有广阔前景.海水中主要离子的含量如下:
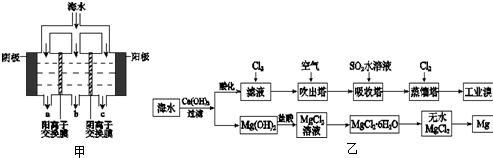
(1)电渗析法淡化海水示意图如图甲所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
①阳极主要电极反应式是
②在阴极附近产生少量白色沉淀,其成分有
③淡水的出口为
(2)利用海水可以提取溴和镁,提取过程如图乙所示:
①提取溴的过程中,经过2次Br-→Br2转化的目的是
②从MgCl2溶液中得到MgCl2?6H2O晶体的主要操作是
③依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
查看习题详情和答案>>
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42 | 2560 | Br- | 64 |
| Mg2+ | 1272 |

(1)电渗析法淡化海水示意图如图甲所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
①阳极主要电极反应式是
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.②在阴极附近产生少量白色沉淀,其成分有
Mg(OH)2
Mg(OH)2
和CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O
Ca2++OH-+HCO3-=CaCO3↓+H2O
.③淡水的出口为
b
b
(填“a”、“b”或“c”).(2)利用海水可以提取溴和镁,提取过程如图乙所示:
①提取溴的过程中,经过2次Br-→Br2转化的目的是
对溴元素进行富集
对溴元素进行富集
,吸收塔中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-
SO2+Br2+2H2O=4H++2Br-+SO42-
.解释通空气的目的是通入空气将Br2蒸气带出,使Br2(g)?Br2(aq)或Br2+H2O?HBr+HBrO平衡向左移动
通入空气将Br2蒸气带出,使Br2(g)?Br2(aq)或Br2+H2O?HBr+HBrO平衡向左移动
.②从MgCl2溶液中得到MgCl2?6H2O晶体的主要操作是
加热浓缩、冷却结晶
加热浓缩、冷却结晶
、过滤、洗涤、干燥.③依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
179.2
179.2
L(忽略Cl2溶解).实验室里用如图示出的装置制取溴化亚铁.其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉.实验开始时先将铁粉加热至600~700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴滴入100~120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g.
 (1)如何检查D装置的气密性?
(1)如何检查D装置的气密性?
(2)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为
(3)在A中盛有CaCO3,a中盛有6mol?L-1盐酸.为使A中产生的CO2在进入D之前既干燥又纯净,B、C处应设置和各仪器中应盛有何种试剂?
(4)实验时,D和E的橡胶塞为什么最好用铝箔包住?
(5)反应过程中要不断地通入CO2,其主要作用是:①
(6)E中进行的反应是:2Fe+3Br2=2FeBr3,2FeBr3=2FeBr2+Br2↑.此实验中溴化亚铁的产率为
(7)为防止污染空气,实验时应在F处连接盛有
查看习题详情和答案>>
 (1)如何检查D装置的气密性?
(1)如何检查D装置的气密性?(2)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为
3Fe+4H2O
Fe3O4+4H2↑
| ||
3Fe+4H2O
Fe3O4+4H2↑
.
| ||
(3)在A中盛有CaCO3,a中盛有6mol?L-1盐酸.为使A中产生的CO2在进入D之前既干燥又纯净,B、C处应设置和各仪器中应盛有何种试剂?
B处应设置盛有NaHCO3饱和溶液的洗气瓶
B处应设置盛有NaHCO3饱和溶液的洗气瓶
C处应设置盛有浓H2SO4的洗气瓶
C处应设置盛有浓H2SO4的洗气瓶
.(4)实验时,D和E的橡胶塞为什么最好用铝箔包住?
因Br2会腐蚀橡胶塞
因Br2会腐蚀橡胶塞
(5)反应过程中要不断地通入CO2,其主要作用是:①
将容器中的空气赶净
将容器中的空气赶净
②将Br2蒸气带入反应器D中
将Br2蒸气带入反应器D中
.(6)E中进行的反应是:2Fe+3Br2=2FeBr3,2FeBr3=2FeBr2+Br2↑.此实验中溴化亚铁的产率为
37.04%
37.04%
.(7)为防止污染空气,实验时应在F处连接盛有
NaOH溶液
NaOH溶液
的尾气吸收装置.
利用海水制取溴(Br2)的流程可表示如下:

含Br-的海水含Br-的海水含Br2的海水蒸发浓缩①酸化②通Cl2③通空气和水蒸气④Br2蒸气H2SO4HBr溶液混合溶液SO2水溶液⑤通Cl2⑥CCl4⑦水溶液Br2/CCl4
(1)完成⑤中反应的化学方程式 .
(2)操作(7)是 .
(3)①②③④⑤操作的目的是 .(选填序号)
a.制取硫酸 b.制取盐酸 c.提纯溴离子 d.富集溴. 查看习题详情和答案>>

含Br-的海水含Br-的海水含Br2的海水蒸发浓缩①酸化②通Cl2③通空气和水蒸气④Br2蒸气H2SO4HBr溶液混合溶液SO2水溶液⑤通Cl2⑥CCl4⑦水溶液Br2/CCl4
(1)完成⑤中反应的化学方程式
(2)操作(7)是
(3)①②③④⑤操作的目的是
a.制取硫酸 b.制取盐酸 c.提纯溴离子 d.富集溴. 查看习题详情和答案>>
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:

请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N 、B .
(2)写出反应②的化学方程式
(3)写出反应③的离子方程式: ,
Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为 .
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 .
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因: .
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 .
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有 性.
(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适? (填“甲”或“乙”),理由是 . 查看习题详情和答案>>

请根据以上信息回答下列问题:
I(1)写出N的化学式和B的名称:N 、B .
(2)写出反应②的化学方程式
(3)写出反应③的离子方程式: ,
Ⅱ粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为 .
A.②③④①B.③④②①C.④③②①D.③②④①
Ⅲ提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2.
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 .
A.分解反应B.化合反应C.置换反应 D.复分解反应
(2)氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体.但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩.试用化学反应方程式解释不选用氮气的原因: .
(3)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 .
A.从外地购买B.在当地新建生产厂
C.从本厂生产烧碱处循环D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有 性.
(4)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适? (填“甲”或“乙”),理由是 . 查看习题详情和答案>>