网址:http://m.1010jiajiao.com/timu_id_3778733[举报]
(14分)(1)向1 L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,则原溶液中Fe3+的物质的量浓度为 ,AlCl3的物质的量 。
(2)已知:2Fe3++2I- = 2Fe2++ I2; 2Fe2++Br2 = 2Fe3++2Br-
①向含有1mol FeI2和1.5mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是 。
②如果向①的溶液中通入3mol Cl2,则被氧化的离子对应的氧化产物分别是 。
(3)①若m g铁屑与含有 n gHNO3的硝酸溶液恰好完全反应,若 m : n =" 1" : 2.7, 该反应的化学方程式为 __________________________________________________(假设还原产物只有一种,且只生成一种盐)
②若含 n g HNO3的稀硝酸溶液恰好使5.6g铁粉完全溶解,若有 n/4 gHNO3被还原成NO(无其它还原产物)则 n 的范围为_________________________
③某条件下锌和硝酸反应时的物质的量之比为2:5,此时硝酸的还原产物是____________
查看习题详情和答案>>
A.m=l,n=6
B.m=1,n=7
C.m=2,n=6
D.m=2,n=7
查看习题详情和答案>>
化学式为C5H12O2的二元醇有多种同分异构体,其中主链上碳原子数为3的同分异构体的数目为m,主链上碳原子数为4的同分异构体的数目为n。下列各组数据中,m和n均正确的是(不包括1个碳原子上连接2个羟基的化合物)
A.m=l,n=6
B.m=1,n=7
C.m=2,n=6
D.m=2,n=7
查看习题详情和答案>>
(1)海水晒盐的原理是:
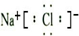
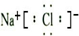
(2)晒出的粗盐常混有MgSO4,CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,②
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+,Cr3+等,为富集镁使其转化力MgCl2晶体.
有关资料:
| M(OH)n | pH | |
| 开始沉淀 | 沉淀完全 | |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mg(OH)2 | 9.5 | 11.0 |
| Cr(OH)3 | 4.3 | 5.0 |
①先加
②再加
③过滤后,为能得到纯净MgCl2晶体,采用的操作方法是:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | F | H | |||||
| 3 | B | C | E | G |
(1)单质中氧化性最强的是
(2)最高价氧化物对应水化物的酸性最强的酸是
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是
(4)D、E、F三种元素按原子半径由大到小的顺序排列为
(5)A的氧化物常温下呈