摘要:1. C,2.B.C,3.C,4.D,5.C.D, 讲析:1.只有NaClO符合3条要求.2.漂白粉是CaCl2和Ca(C10)2的混合物.但其有效成分为Ca(C10)2.A错,漂白粉在空气中发生以下反应而变质: Ca(C10)2+H20+CO2=CaCO3+2HClO, 2HclO=2HCl+02↑ .B正确,Ca(C10)2为强碱弱酸盐.水解后显碱性.C正确.漂白粉使用时不能使用浓盐酸.因为要发生氧化还原反应: Ca(C10)2+4HCl(浓)=CaCl2+Cl2↑+2H20. D错. Δ == 3.盐酸中n(HCl)=0.6mol.由实验室制取Cl2 的反应:MnO2+4HCl MnCl2+Cl2↑+2H20可知MnO2过量.则0.6molHCl中最多有0.3mol被氧化.但实际上随着反应的进行.盐酸的浓度变稀.被氧化的HCl必然小于0.3mol.即溶液中Cl-的量必然大于0.3 mol.产生的AgCl的量大于0.3mol.当然小于0.6mol. 4.本题可采用“极值法 .显然H2.Cl2混合气体中Cl2的量越大.消耗的NaOH的量就越大.反之越小.Cl2的极限为aL.此时消耗NaOH物质的量为a/11.2.因Cl2的体积总是小于aL.故答案为D. 5.液氯为单质.氯水为混合物.二者既不是电解质又不是非电解质.不干燥的氯气遇二氧化硫发生反应:SO2+Cl2+2H2O==2HCl+H2SO4.二者漂白性能均减弱.A.B的结论均正确.
网址:http://m.1010jiajiao.com/timu_id_3777649[举报]
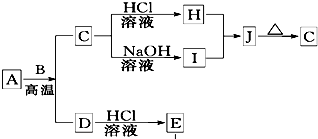 B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.
B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.(1)在E的溶液中加入氢氧化钠溶液,可以观察到的现象是
先生成白色沉淀,迅速变为灰绿色,最终变为红褐色
先生成白色沉淀,迅速变为灰绿色,最终变为红褐色
.(2)按要求写化学方程式或离子方程式:
①A与B在高温条件下生成C和D的化学方程式:
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
;
| ||
②在E的水溶液中通入氯气后的生成物和I溶液反应的离子方程式:
Fe3++3AlO2-+6H2O═3Al(OH)3↓+Fe(OH)3↓
Fe3++3AlO2-+6H2O═3Al(OH)3↓+Fe(OH)3↓
.(3)由D和A组成的混合物与稀HCl作用,固体恰好溶解,所得溶液中滴加KSCN溶液不显红色,且生成的E与H2的物质的量之比为4:1.则反应物中A、D、HCl的物质的量之比为
1:2:8
1:2:8
.A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别位于同一主族,A是自然界中原子半径最小的元素,B的最外层电子数是内层电子数的3倍.
(1)写出B的元素符号:B
 ;
;
(2)B与D的氢化物较稳定的是
(3)写出C2B2的电子式
 ;写出实验室制取DB2的化学方程式:
;写出实验室制取DB2的化学方程式:
(4)写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式
查看习题详情和答案>>
(1)写出B的元素符号:B
O
O
,C的原子结构示意图

(2)B与D的氢化物较稳定的是
H2O
H2O
(填化学式),其中所含有的化学键类型为极性键
极性键
;(3)写出C2B2的电子式


Na2SO3+H2SO4═Na2SO4+H2O+SO2↑
Na2SO3+H2SO4═Na2SO4+H2O+SO2↑
(4)写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式
HSO3-+H+=SO2↑+H2O
HSO3-+H+=SO2↑+H2O
.a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg5种金属中的一种.已知:(1)a、c均能与稀硫酸反应放出气体;(2)b与d的硝酸盐反应,置换出单质d;(3)c与强碱反应放出气体;(4)c、e在冷浓硫酸中发生钝化.由此可判断a、b、c、d、e依次为( )
查看习题详情和答案>>
A、B、C、D、E、F 6种主族元素,它们的原子序数依次增大.已知A、C、F三种元素的原子最外层共有10个电子,且这三种元素的最高价氧化物的水化物之间能两两发生反应都生成盐和水;又知D元素的原子最外层电子数比次外层电子数少4,E元素原子的次外层电子数比最外层电子数多3.请填写下列空白处:
(1)元素的符号:A.
(2)元素B和F形成的化合物的电子式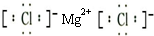
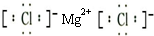 .
.
(3)D元素的氧化物属于
(4)E元素的最高价氧化物与水反应的化学方程式是
查看习题详情和答案>>
(1)元素的符号:A.
Na
Na
,C.Al
Al
.(2)元素B和F形成的化合物的电子式
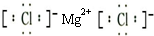
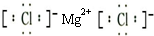
(3)D元素的氧化物属于
原子
原子
晶体,含a mol D的上述晶体中含D-O共价键4a
4a
mol.(4)E元素的最高价氧化物与水反应的化学方程式是
P2O5+3H2O=2H3PO4
P2O5+3H2O=2H3PO4
.A、B、C、D是中学化学常见的四种短周期元素,已知:
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为
 ,Y与水反应产物的化学式为
,Y与水反应产物的化学式为
查看习题详情和答案>>
①A元素原子最外层电子数是次外层电子数的2倍,且A与D同主族;
②B元素最高正价与负价的代数和为2;
③C元素有多种化合价,且常温下C元素的气态单质与NaOH溶液反应,可得两种含C元素的化合物;
④B、C两种元素质子数之和是A元素质子数的4倍.
(1)A、B、C三种元素最高价氧化物对应水化物的酸(碱)性由强到弱的顺序是(用化学式表示)
HClO4>HNO3>H2CO3
HClO4>HNO3>H2CO3
,D元素在元素周期表中的位置是第三周期ⅣA族
第三周期ⅣA族
(2)B的最高价氧化物的水化物的稀溶液与铜单质反应,离子方程为
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
,现有19.2g 铜粉溶解,产生标准状况下气体的体积是4.48
4.48
L.(3)B、D两元素可形成一种新型无机非金属化合物材料X.X可由C、D两元素形成的化合物Z与B的氢化物在一定条件下制得,则生成X的化学方程为
3SiCl4+4NH3═Si3N4+12HCl
3SiCl4+4NH3═Si3N4+12HCl
.(4)由B、C两种元素组成的化合物Y,常温下为易挥发的淡黄色液体,Y分子为三角锥形分子,且B、C两种原子最外层均达到8个电子的稳定结构.Y遇水蒸气可生成一种常见的漂白性物质.则Y的电子式为


NH3和HClO
NH3和HClO
.