摘要: ⑴ 从图中可以看出.1mol混合烃完全燃烧生成CO2比H2O的物质的量少0.4mol, ⑵ ①CH4.C2H4 2∶3 ②CH4.C3H4 7∶3 ③CH4.C4H4 4∶1
网址:http://m.1010jiajiao.com/timu_id_3747670[举报]
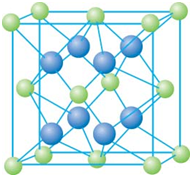 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答:
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答:(1)A元素的名称是
氢
氢
;(2)B元素的轨道表示式是
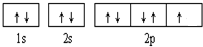


氟化氢分子间存在氢键,氯化氢分子间没有氢键
氟化氢分子间存在氢键,氯化氢分子间没有氢键
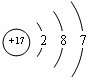
;(3)E属于元素周期表中第
四
四
周期,第VIIB
VIIB
族的元素,其元素名称是锰
锰
;属于元素周期表中的d
d
区(填元素分区),它的+2价离子的电子排布式为1s22s22p63s23p63d5
1s22s22p63s23p63d5
;(4)从图中可以看出,D跟B形成的离子化合物的化学式为
CaF2
CaF2
;该离子化合物晶体的密度为a g?cm-3,则晶胞的体积是| 4×78g/mol |
| ag/cm3×6.02×1023/mol |
| 4×78g/mol |
| ag/cm3×6.02×1023/mol |
 如图所示标出了各种材料强度与密度的比值以及广泛使用的年代.从图中可以看出的信息有( )
如图所示标出了各种材料强度与密度的比值以及广泛使用的年代.从图中可以看出的信息有( )| A、科学技术的发展越来越快,新材料频频出现 | B、新材料发展的总体趋势是强度越来越大 | C、1800年以前出现的材料强度都比铝小 | D、铝的密度比钢的密度大 |
 (1)美国“阿特兰蒂斯号”航天飞机与2009年5月11日升空修复含勃望远镜,它使用的燃料是液氢和液氧.已知下列热化学方程式:
(1)美国“阿特兰蒂斯号”航天飞机与2009年5月11日升空修复含勃望远镜,它使用的燃料是液氢和液氧.已知下列热化学方程式:H2(l)+
| 1 | 2 |
H2O(l)=H2O(g);△H=+44.0kJ/mol
请写出液氢和液氧生成气态水的热化学方程式:
(2)在利用CaCO3与盐酸反应制取二氧化碳的反应中,反应中生成二氧化碳的体积与反应的时间关系如图所示,两个实验所用的盐酸浓度相同,其中一个实验用的是石灰石块,另一实验用的是石灰石粉末,则从图中可以看出:使用石灰石块的是
(3)已知反应X(g)+2Y(g)?2Z(g),如右图所示,相同温度下,在甲、乙两容器中各投入1mol X、2mol Y和适量催化剂,甲乙两容器的初始体积均为1L,乙活塞可自由滑动.甲、乙 达到平衡所用时间:甲
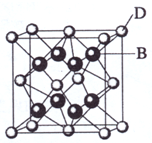 (2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.
(2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.请回答:
(1)A元素的名称是
氢
氢
;(2)B的元素符号是
F
F
,C的元素符号是Cl
Cl
,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是氟化氢分子间存在氢键,氯化氢分子间没有氢键
氟化氢分子间存在氢键,氯化氢分子间没有氢键
(3)E属元素周期表中第
四
四
周期,第VIIB
VIIB
族的元素,其元素名称是锰
锰
,它的+2价离子的电子排布式为1s22s22p63s23p63d5
1s22s22p63s23p63d5
:(4)从图中可以看出,D跟B形成的离子化合物的化学式为
CaF2
CaF2
;该离子化合物晶体的密度为a g?cm-3,则晶胞的体积是| 4×78g/mol |
| ag?cm-3×6.02×1023/mol |
| 4×78g/mol |
| ag?cm-3×6.02×1023/mol |
