摘要:21.(1)100 mL容量瓶 (2)> b (3)配制pH=1的HA溶液难以实现 不妥之处在于加入的粒难以做到表面积相同 (4)配制NaA溶液.测其pH>7即证明HA是弱电解质
网址:http://m.1010jiajiao.com/timu_id_3248118[举报]
(实验室欲配制100mL2mol/L的NaCl溶液,请回答:
(1)配制时用托盘天平称量NaCl固体
(2)配制过程中需要的仪器有:药匙、托盘天平和砝码、烧杯、
(3)选出所需的操作并写出正确的操作顺序
A.计算 B.称量 C.洗涤 D.定容
E.溶解 F.摇匀 G.转移
(4)定容的正确操作是:继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改用胶头滴管向容量瓶滴加蒸馏水至
(5)由于操作不当,会引起实验误差.下列情况对所配制的NaCl溶液的物质的量浓度有何影响?(用“偏大”、“偏小”、无影响填写):
①加水定容时超过刻度线
②容量瓶用蒸馏水洗涤后残留有少量的水
③摇匀后,发现溶液的液面低于刻度线,又加水至刻度线
(6)容量瓶上标有
①温度 ②浓度 ③体积
④压强 ⑤刻度线 ⑥酸式或碱式.
查看习题详情和答案>>
(1)配制时用托盘天平称量NaCl固体
11.7
11.7
g.(2)配制过程中需要的仪器有:药匙、托盘天平和砝码、烧杯、
100 mL容量瓶
100 mL容量瓶
、玻璃棒
玻璃棒
、胶头滴管
胶头滴管
.(3)选出所需的操作并写出正确的操作顺序
ABEGCGDF
ABEGCGDF
(选填下列字母).A.计算 B.称量 C.洗涤 D.定容
E.溶解 F.摇匀 G.转移
(4)定容的正确操作是:继续向容量瓶注入蒸馏水至离刻度线1-2cm处,改用胶头滴管向容量瓶滴加蒸馏水至
凹液面与刻度线相切
凹液面与刻度线相切
为止.(5)由于操作不当,会引起实验误差.下列情况对所配制的NaCl溶液的物质的量浓度有何影响?(用“偏大”、“偏小”、无影响填写):
①加水定容时超过刻度线
偏小
偏小
;②容量瓶用蒸馏水洗涤后残留有少量的水
无影响
无影响
;③摇匀后,发现溶液的液面低于刻度线,又加水至刻度线
偏小
偏小
.(6)容量瓶上标有
①③⑤
①③⑤
(填写编号)①温度 ②浓度 ③体积
④压强 ⑤刻度线 ⑥酸式或碱式.
某同学用胆矾固体(CuSO4?5H2O )配制0.30mol/L的CuSO4溶液100mL,回答下列问题
(1)所需仪器为:容量瓶、托盘天平、药匙、胶头滴管,还需要那些玻璃仪器才能完成该实验,请写出:
(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾
③
(3)称量的操作顺序为(填序号)
A、调天平零点 B、游码回零
C、向小烧杯中加入碳酸钠 D、称量空烧杯
E、向右盘加砝码并把游码移到所需位置 F、将砝码回盒
G、记录称量结果
(4)如图是该同学转移溶液的操作示意图,图中的错误是:
(5)下列操作会使所配溶液的浓度偏高的是
A、称量时所用砝码已生锈
B、往容量瓶转移溶液时,有少量液体溅出
C、胆矾已失去部分结晶水
D、未洗涤溶解胆矾的烧杯
E、定容时,俯视刻度线
F、小烧杯洗净后未干燥即用来称量
G、容量瓶未干燥即用来配制溶液
H、该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.
查看习题详情和答案>>
(1)所需仪器为:容量瓶、托盘天平、药匙、胶头滴管,还需要那些玻璃仪器才能完成该实验,请写出:
烧杯、玻璃棒
烧杯、玻璃棒
.(2)请写出该实验的简要的实验步骤:
①计算 ②称量胆矾
7.5
7.5
g③
溶解
溶解
④转移 ⑤洗涤并转移 ⑥定容 ⑦摇匀(3)称量的操作顺序为(填序号)
BADGECF
BADGECF
.A、调天平零点 B、游码回零
C、向小烧杯中加入碳酸钠 D、称量空烧杯
E、向右盘加砝码并把游码移到所需位置 F、将砝码回盒
G、记录称量结果

(4)如图是该同学转移溶液的操作示意图,图中的错误是:
未用玻璃棒引流; 未采用100 mL容量瓶
未用玻璃棒引流; 未采用100 mL容量瓶
.(5)下列操作会使所配溶液的浓度偏高的是
ACE
ACE
.A、称量时所用砝码已生锈
B、往容量瓶转移溶液时,有少量液体溅出
C、胆矾已失去部分结晶水
D、未洗涤溶解胆矾的烧杯
E、定容时,俯视刻度线
F、小烧杯洗净后未干燥即用来称量
G、容量瓶未干燥即用来配制溶液
H、该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.
配制一定物质的量浓度溶液时,下列有关实验操作或判断正确的是( )
| A、配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小 | B、需要95 mL 0.1 mol?L-1 NaCl溶液,可选用100 mL容量瓶来配制 | C、用100mL的量筒量取5.20mL的盐酸 | D、配制一定物质的量浓度溶液时,容量瓶水洗后可不干燥 |
某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
请回答下列问题:
Ⅰ.(1)实验时用18.4 mol·L-1的浓硫酸,配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为 。(计算结果精确到小数点后一位)
(2)下列操作中,容量瓶所具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液
C.用来溶解固体溶质 D.常用来代替量筒量取一定体积的液体
(3)在下列配制过程示意图中,有错误的是(填写序号) 。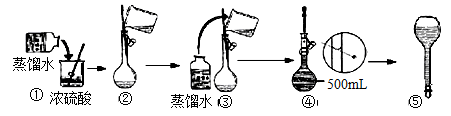
(4)下列说法正确的
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
Ⅱ.(1)步骤②加入过量H2O2的目的: 。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a. ,b. 洗涤,c. 灼烧,d. 冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为 。
Ⅲ.已知人体不能很好地吸收利用Fe3+,科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C,以利于铁元素的吸收。试分析维生素C在这一过程中的作用是 。