摘要:W 氢氧化物开始沉淀时的pH氢氧化物沉淀完全时的pHCu2+
网址:http://m.1010jiajiao.com/timu_id_302095[举报]
(2013?太原模拟)在溶液中有浓度均为0.01mol?L-1的Fe3+、Cr3+、Zn2+、Mg2+等离子,已知:
Ksp[Fe(OH)3]=2.6×10-39; Ksp[Cr(OH)3]=7.0×10-31;
Ksp[Zn(OH)2]=1.0×10-17; Ksp[Mg(OH)2]=1.8×10-11;
当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小( )
Ksp[Fe(OH)3]=2.6×10-39; Ksp[Cr(OH)3]=7.0×10-31;
Ksp[Zn(OH)2]=1.0×10-17; Ksp[Mg(OH)2]=1.8×10-11;
当氢氧化物开始沉淀时,下列哪一种离子所需溶液的pH最小( )
查看习题详情和答案>>
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3和SiO2组成.某实验小组设计如图甲流程欲分别制得单质Al、Fe、Mg和Si.

有关氢氧化物沉淀的pH见下表:
(1)写出不溶物B在生产中的一种用途:
(2)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
a. NaOH溶液 b.氨水 c. MgO d. Mg (OH)2
(3)从滤液H制取金属Mg的流程如图乙:
Ⅰ.流程中由滤液H中得到MgCl2?6H2O的方法是
Ⅱ.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是
Ⅲ.冶炼镁的方法用化学方程式表示为
查看习题详情和答案>>

有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
制造玻璃、光导纤维
制造玻璃、光导纤维
.(2)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
cd
cd
.a. NaOH溶液 b.氨水 c. MgO d. Mg (OH)2
(3)从滤液H制取金属Mg的流程如图乙:
Ⅰ.流程中由滤液H中得到MgCl2?6H2O的方法是
蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶
过滤、洗涤;Ⅱ.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是
Mg2++2H2O?Mg(OH)2+2H+,通入HCl,使C(H+)增大,抑制Mg2+的水解成Mg(OH)2,确保生成MgCl2
Mg2++2H2O?Mg(OH)2+2H+,通入HCl,使C(H+)增大,抑制Mg2+的水解成Mg(OH)2,确保生成MgCl2
.(应用离子方程式和简要文字说明)Ⅲ.冶炼镁的方法用化学方程式表示为
MgCl2
Mg+Cl2↑
| ||
| 熔融 |
MgCl2
Mg+Cl2↑
.
| ||
| 熔融 |
(2009?丹东模拟)蛇纹石矿可以看作由MgO、Fe2O3、Al2O3和SiO2组成.某实验小组设计如下流程欲分别制得单质Al、Fe、Mg和Si.

有关氢氧化物沉淀的pH见下表:
请回答下列问题:
(1)滤液A中含有的阳离子有
(2)操作②中涉及的化学方程式为
操作④中生成沉淀G的离子方程式为
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
a.NaOH溶液 b.氨水 c.MgO d.Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:

流程中由MgCl2冶炼Mg的方法是
查看习题详情和答案>>

有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(1)滤液A中含有的阳离子有
Fe3+、Al3+、Mg2+、H+
Fe3+、Al3+、Mg2+、H+
.(2)操作②中涉及的化学方程式为
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
,
| ||
操作④中生成沉淀G的离子方程式为
AlO-2+CO2+2H2O═Al(OH)3↓+HCO-3
AlO-2+CO2+2H2O═Al(OH)3↓+HCO-3
.(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
cd
cd
.a.NaOH溶液 b.氨水 c.MgO d.Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:

流程中由MgCl2冶炼Mg的方法是
电解
电解
.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是防止Mg2+水解,并带走水分
防止Mg2+水解,并带走水分
.(2013?聊城一模)白云石的主要成分为CaCO3?MgCO3,还含有少量Fe、Si的化合物.实验室以白云石为原料制备Mg(OH)2及CaCO3.步骤如下:

实验过程中需要的数据见下表:
请回答下列问题:
(1)过滤中所需的玻璃仪器是
A.KMnO4 B.Cl2 C.H2O2
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是
 (不允许更换溶液,导气管以下连接的仪器自选)
(不允许更换溶液,导气管以下连接的仪器自选)
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为
(4)若将制取的Mg(OH)2加入到某聚乙烯树脂中Mg(OH)2,树脂可燃性大大降低,Mg(OH)2起阻燃作用的主要原因是
查看习题详情和答案>>

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
(1)过滤中所需的玻璃仪器是
烧杯、玻璃棒、漏斗
烧杯、玻璃棒、漏斗
,溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择BC
BC
(填字母,下同).A.KMnO4 B.Cl2 C.H2O2
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是
NH3
NH3
,然后通入CO2.通入CO2气体时请把装置图补充完整


(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为
Ksp[Fe(OH)3]<Ksp[Fe(OH)2]<Ksp[Mg(OH)2]
Ksp[Fe(OH)3]<Ksp[Fe(OH)2]<Ksp[Mg(OH)2]
.(4)若将制取的Mg(OH)2加入到某聚乙烯树脂中Mg(OH)2,树脂可燃性大大降低,Mg(OH)2起阻燃作用的主要原因是
Mg(OH)2受热分解时吸收大量的热,使环境温度下降;同时生成耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳
Mg(OH)2受热分解时吸收大量的热,使环境温度下降;同时生成耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳
.(2012?闸北区二模)某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl2?2H2O晶体的工艺流程如下:
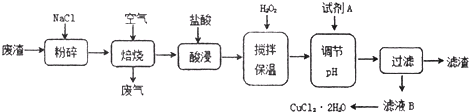
己知:①焙烧过程中发生的主要反应为:CuS+2NaCl+2O2→CuCl2+Na2SO4
请参照表中给出的数据回答:
(1)焙烧时还有废气产生,其中一种是主要的大气污染物.若在实验室中以碱液吸收处理之,下列(图1)A、B、C装置中可行的是
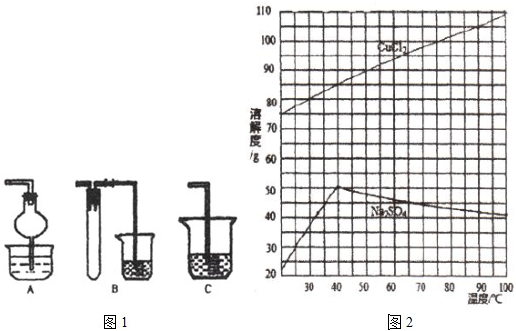
(2)H2O2的作用是:
(3)调节溶液pH的范围是
a.KOH b.氨水
c.Cu2(OH)2CO3 d.CuO
(4)为了获得CuCl2?2H2O晶体,对滤液B进行的操作是:
(5)滤液B中除OH-外阴离子还有
(6)请描述检验滤液B中上述阴离子(除OH-外)的实验操作
查看习题详情和答案>>

己知:①焙烧过程中发生的主要反应为:CuS+2NaCl+2O2→CuCl2+Na2SO4
请参照表中给出的数据回答:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
AB
AB
(填字母).
(2)H2O2的作用是:
氧化Fe2+
氧化Fe2+
.(3)调节溶液pH的范围是
3.2至4.7
3.2至4.7
,试剂A可以选择cd
cd
(填写选项字母).a.KOH b.氨水
c.Cu2(OH)2CO3 d.CuO
(4)为了获得CuCl2?2H2O晶体,对滤液B进行的操作是:
蒸发浓缩
蒸发浓缩
,趁热过滤,滤液经冷却结晶,过滤得到产品.分析有关物质的溶解度曲线(如图2),“趁热过滤”得到的固体是Na2SO4
Na2SO4
(填化学式).(5)滤液B中除OH-外阴离子还有
S042- Cl-
S042- Cl-
.(6)请描述检验滤液B中上述阴离子(除OH-外)的实验操作
取少量滤液,先加过量的硝酸酸化的Ba(NO3)2溶液,有白色沉淀出现,检出SO42-;过滤(或静置)再向滤液(或清液)加入适量的AgNO3溶液,也有白色沉淀出现,检出Cl-
取少量滤液,先加过量的硝酸酸化的Ba(NO3)2溶液,有白色沉淀出现,检出SO42-;过滤(或静置)再向滤液(或清液)加入适量的AgNO3溶液,也有白色沉淀出现,检出Cl-
.