摘要:20.0 0.125mol 150
网址:http://m.1010jiajiao.com/timu_id_213567[举报]
硫酸铜是一种重要的化工原料,工业上常用硫酸为原料来制备硫酸铜.
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源.为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4.写出该反应的化学方程式 ;
实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是 .
(2)测定硫酸铜晶体中结晶水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重;
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重;
步骤5: ;
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数.
请完成实验步骤5.
(3)已知硫酸铜晶体受热可以逐步失去结晶水,温度升高还可以分解生成铜的氧化物.取25.0g CuSO4?5H2O 晶体均匀受热,缓慢升温至1 200℃并恒温1小时,实验测得固体残留率(
×100%)与温度的关系如图所示:
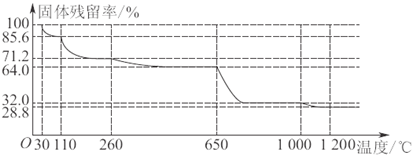
在110℃时所得固体的成分为 ;
在1 200℃并恒温1小时,反应所得气态产物除去水后,物质的量为 .(填字母)
A.0mol B.0.1mol C.0.125mol D.大于0.125mol. 查看习题详情和答案>>
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源.为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4.写出该反应的化学方程式
实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是
(2)测定硫酸铜晶体中结晶水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重;
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重;
步骤5:
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数.
请完成实验步骤5.
(3)已知硫酸铜晶体受热可以逐步失去结晶水,温度升高还可以分解生成铜的氧化物.取25.0g CuSO4?5H2O 晶体均匀受热,缓慢升温至1 200℃并恒温1小时,实验测得固体残留率(
| 剩余固体的质量 | 原始固体质量 |

在110℃时所得固体的成分为
在1 200℃并恒温1小时,反应所得气态产物除去水后,物质的量为
A.0mol B.0.1mol C.0.125mol D.大于0.125mol. 查看习题详情和答案>>
在铜锌原电池中,浓度为0.125mol/L的硫酸溶液200ml,若工作一段时间后,从装置中共收集到0.168L(标准状况)气体,求:(1)通过导线的电子的物质的量
(2)此时溶液中H+的物质的量浓度.(假若溶液的体积变化忽略不计)
查看习题详情和答案>>
(2)此时溶液中H+的物质的量浓度.(假若溶液的体积变化忽略不计)
在标准状况下,将CO2和CO的混合气体(标准状况下,该混合气体平均相对分子质量为32)充满一盛有足量Na2O2的容积为22.4L的密闭容器中,用间断的电火花引发至充分反应.反应完全后容器里的存在物叙述正确的是( )
| A、存在0.5mol的CO | B、存在0.25mol的Na2CO3 | C、存在0.125mol的O2 | D、存在0.75mol的Na2CO3 |
(2013?长宁区一模)温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
|
查看习题详情和答案>>