摘要:A.NH3(g)+O2(g)NO(g)+H2O(g), ΔH=-a kJ?mol-1
网址:http://m.1010jiajiao.com/timu_id_209337[举报]
一、选择题(共55分)(其中1―5每题2分共10分,6―20每题3分共45分)
1―5 BBCDB 6―10 DBBBA 11―15 BCBAB 16―20 CCCBD
二、填空题
21.(10分)(1)A:碳酸铵或碳酸氢铵(2分)
B:略 D:三角锥 G:红棕色(各1分)
(2)2CO2+2Na2O2=2Na2CO3+O2↑(2分)
(3)4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H=+108akJ?mol-1(3分)
(1)4HCl(浓盐酸)+MnO2===MnCl2+2H2O+Cl2↑(2分)
.files/image022.gif) |
(2)2Cl2+2H2O(气)+C====4HCl↑+CO2↑(2分)
吸收Cl2中的HCl气体,提供D处所需水蒸气。(1分)
(3)生成的HCl气体使紫石蕊溶液变红,因未反应完的Cl2与H2O作用产生的HClO的漂白作用使红色消失。(2分)
(4)B(1分)
(5)瓶中液面下降,长颈漏斗内液面上升;贮存少量Cl2(2)
23.(11分)(1)0.93<x(Mg)<1.57,2,55<x(N)<3.44。(各2分)
(2)同周期(同主族)中,x值越大,其原子半径越小;(2分)周期性。(1分)
(3)氮原子(1分)
(4)共价键(2分)
(5)第六周期IA族(1分)
24.(9分)(1)正向(1分) (2)B、D(2分)
(3)①n(D)>0.6mol(2分)②n(C)=1.8mol n(D)>0.5mol(各2分)
三、计算题(5分)
26.(1)66.7% (2)50
硝酸铵在工农业生产和国防中占有极为重要的位置,下面的流程图是硝酸铵的工业生产工艺过程.
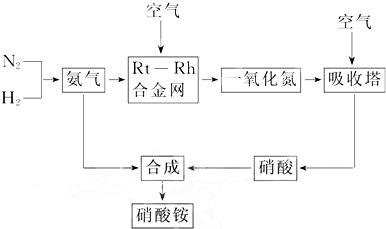
根据图回答下列问题:(1)已知N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.请回答:①在500℃、1.01×105 kPa和铁催化条件下向一密闭容器中充入1 mol N2和3 mol H2,充分反应后,放出的热量小于92.4 kJ,理由:②为有效提高氢气的转化率,实际生产中宜采取的措施有.A.降低压强B.最适合催化剂活性的适当高温C.增大压强D.及时移出氨E.循环利用和不断补充氮气(2)氨催化氧化的化学方程式为4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0.
该反应的化学平衡常数表达式K=
,当温度升高时,K值
查看习题详情和答案>>

根据图回答下列问题:(1)已知N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.请回答:①在500℃、1.01×105 kPa和铁催化条件下向一密闭容器中充入1 mol N2和3 mol H2,充分反应后,放出的热量小于92.4 kJ,理由:②为有效提高氢气的转化率,实际生产中宜采取的措施有.A.降低压强B.最适合催化剂活性的适当高温C.增大压强D.及时移出氨E.循环利用和不断补充氮气(2)氨催化氧化的化学方程式为4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0.
该反应的化学平衡常数表达式K=
| c4(NO)?c6(H2O) |
| c4(NH3)?c5(O2) |
| c4(NO)?c6(H2O) |
| c4(NH3)?c5(O2) |
减小
减小
(填“增大”“减小”或“无影响”).工业制硝酸的主要反应是:4NH3(g)+5O2(g)?4NO(g)+6H2O (g)+1025kJ
(1)该反应的平衡常数表达式为K=
;升高温度K值
(2)若反应物起始的物质的量相同,如图所示关系图错误的是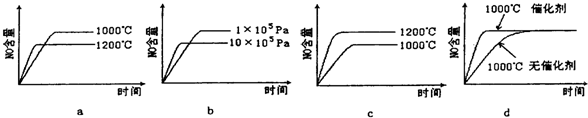
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①起始时物料比c(O2):c(NH3)>1.25,其原因是
②反应在第2min到第4min时O2的平均反应速率为
③反应在第2min改变了反应条件,改变的条件可能是
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是
查看习题详情和答案>>
(1)该反应的平衡常数表达式为K=
| c4(NO)c6(H2O) |
| c4(NH3)c5(O2) |
| c4(NO)c6(H2O) |
| c4(NH3)c5(O2) |
减小
减小
(填“增大”、“减小”或“不变”).(2)若反应物起始的物质的量相同,如图所示关系图错误的是
c
c
(填字母序号).
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 1.6 | 0.5 |
增大氨气的转化率
增大氨气的转化率
.②反应在第2min到第4min时O2的平均反应速率为
0.1875
0.1875
mol/L?min;③反应在第2min改变了反应条件,改变的条件可能是
c
c
(填字母序号).a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是
增大反应物的浓度.
增大反应物的浓度.
. (2011?福建模拟)甲是一元强碱,其阴、阳离子所含电子总数相等.在溶液中能发生下列反应:
(2011?福建模拟)甲是一元强碱,其阴、阳离子所含电子总数相等.在溶液中能发生下列反应:甲+乙
| △ |
Ⅰ.若丙是NH3.
(1)甲与乙溶液反应的离子方程式是
NH4++OH-
NH3↑+H2O
| ||
NH4++OH-
NH3↑+H2O
.
| ||
(2)820℃时,一定量NH3和O2反应生成NO和H2O,反应达到化学平衡.平衡常数K=
| c4(NO)×c6(H2O) |
| c4(NH3)×c5(O2) |
| c4(NO)×c6(H2O) |
| c4(NH3)×c5(O2) |
N2(g)+O2(g)=2NO(g)△H=+180kJ?mol-1
N2(g)+O2(g)=2NO(g)△H=+180kJ?mol-1
.Ⅱ.若乙是由元素X组成的单质,丙、丁都是正盐,且均能使酸性KMnO4溶液褪色.丙中所含阴离子为X2-,X2-的结构示意图为

(3)丙溶液中,c (OH-)
>
>
c (HX-)(填“>”、“<”或“=”);丁的化学式为Na2SO3
Na2SO3
.(4)元素Y与X同主族且位置相邻,H2X(g)、H2Y(g)各1mol发生分解反应(产物除氢气外,另一种物质的状态相同)的反应热分别为+20.6kJ?mol-1、-29.7kJ?mol-1.Y在周期表中的位置是
第4周期ⅥA族
第4周期ⅥA族
..files/image021.gif)
 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )