摘要:(1)Cl2+2I-=2Cl-+I2(2)3HClO3=HClO4+2O2↑+Cl2↑+H2O
网址:http://m.1010jiajiao.com/timu_id_174258[举报]
海带中含有丰富的碘元素(以I-形式存在).实验室中提取碘的流程如下:(已知:Cl2+2KI=2KCl+I2)
(1)提取碘的流程中:步骤①需要的主要仪器是
(2)写出步骤②中涉及的有关离子反应方程式
(3)提取碘的过程中,可供选择的有机试剂有
A.四氯化碳 B.醋酸 C.酒精 D.苯.
查看习题详情和答案>>

(1)提取碘的流程中:步骤①需要的主要仪器是
②
②
,步骤③需要的主要仪器是③
③
(填序号)
(2)写出步骤②中涉及的有关离子反应方程式
Cl2+2I-=I2+2Cl-
Cl2+2I-=I2+2Cl-
.(3)提取碘的过程中,可供选择的有机试剂有
A、D
A、D
.A.四氯化碳 B.醋酸 C.酒精 D.苯.
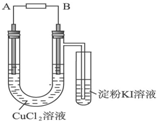 某学生用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,装置如图所示.
某学生用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,装置如图所示.(1)A和B为两石墨电极,则B应与直流电源的
正
正
极相连.(2)写出B电极上电极反应式
2Cl--2e-═Cl2↑
2Cl--2e-═Cl2↑
,试管中淀粉KI溶液变化的现象为变蓝色
变蓝色
,相应的离子方程式为Cl2+2I-═I2+2Cl-
Cl2+2I-═I2+2Cl-
.(3)为精确测定电极上析出铜的质量,有下列实验步骤:
①称量电解前电极质量;
②刮下电解后电极上的铜并清洗;
③用蒸馏水清洗电解后电极;
④低温烘干电极称量;
⑤低温烘干刮下的铜称量;
⑥再次低温烘干后称量到恒重.
实验步骤的先后顺序应是
①③④⑥
①③④⑥
.(4)通电电流为I A,通电t s后精确测得铜的质量为m g,已知电子的电量为1.6×10-19C,试写出阿伏加德罗常数的计算表达式:NA=
| 64It |
| 2m×1.6×10-19 |
| 64It |
| 2m×1.6×10-19 |
如图是一套制取并验证氯气部分化学性质的实验装置.

回答下列问题:反应的方程式:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑
(1)装置A中,仪器a的名称叫
(2)当Cl2气流通过一段时间后,装置B中溶液的pH值
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为_
(4)当Cl2气流持续通过时,装置D中干燥的有色布条能否褪色?为什么?
(5)装置E的作用是
查看习题详情和答案>>

回答下列问题:反应的方程式:MnO2+4HCl(浓)
| ||
(1)装置A中,仪器a的名称叫
分液漏斗
分液漏斗
,该仪器中盛有的试剂为浓盐酸
浓盐酸
.(2)当Cl2气流通过一段时间后,装置B中溶液的pH值
<
<
7(填“>”“<”或“=”),写出Cl2与水反应的方程式Cl2+H2O═HCl+HClO
Cl2+H2O═HCl+HClO
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为_
蓝色
蓝色
色,反应的离子方程式为Cl2+2I -=2Cl-+I2
Cl2+2I -=2Cl-+I2
.(4)当Cl2气流持续通过时,装置D中干燥的有色布条能否褪色?为什么?
不能,因为干燥的氯气没有漂白性
不能,因为干燥的氯气没有漂白性
.(5)装置E的作用是
吸收多余的氯气
吸收多余的氯气
.常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br- ②2Br-+Cl2=Br2+2Cl- ③2Fe3++2I-=2Fe2++I2.由此判断下列说法错误的是( )
查看习题详情和答案>>
下图转化关系中,A、B、C、D、E都是短周期元素的单质,在常温常压下A是固体,其余都是气体,且C呈黄绿色.化合物H和I两种气体相遇时产生白烟.化合物G的焰色反应为黄色.反应①和②均在溶液中进行.

请按要求回答下列问题.
(1)写出下列物质的化学式:D
(2)反应①的离子方程式为
(3)向K溶液中加入硝酸酸化的硝酸银溶液,反应的现象为
(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色.该反应的离子方程式为
查看习题详情和答案>>

请按要求回答下列问题.
(1)写出下列物质的化学式:D
H2
H2
、FNa2O2
Na2O2
.(2)反应①的离子方程式为
2H++CO32-=H2O+CO2
2H++CO32-=H2O+CO2
.(3)向K溶液中加入硝酸酸化的硝酸银溶液,反应的现象为
产生白色沉淀
产生白色沉淀
.(4)将少量单质C通入盛有淀粉KI溶液的试管中,液体变为蓝色.该反应的离子方程式为
Cl2+2I-=I2+2Cl-
Cl2+2I-=I2+2Cl-
.这说明单质C的氧化性强
强
于单质碘(填“强”或“弱”).