摘要:19.下图中.A是由两种常见元素组成的化合物.E是日常生活中常见的金属.K是化学实验中常见的非金属单质.B.F是正四面体结构.且B是一种常见的能源.G.H是工业用途广泛的重要化工原料(图中部分反应物或生成物没有列出) 请按要求回答: (1)写出化学式:A E .写出电子式:F . (2)反应①的化学方程式 . (3)反应②的离子方程式 . (4)反应③的化学方程式 .
网址:http://m.1010jiajiao.com/timu_id_1739989[举报]
下图中,A是由两种常见元素组成的化合物,E是日常生活中常见的金属,K是化学实验中常见的非金属单质,B、F是正四面体结构,且B是一种常见的能源,G、H是工业用涂广泛的重要化工原料(图中部分反应物或生成物没有列出)

请按要求回答:
(1)写出化学式:A________,E________,写出电子式:F________.
(2)反应①的化学方程式________,
(3)反应②的离子方程式________,
(4)反应③的化学方程式________.
化合物A由两种常见元素组成,且A中两种元素的质量比为4:1.A有如图所示转化关系,其中B、F均为红色固体,C能使品红溶液褪色(有的反应可能在水溶液中进行,有的反应的生成物未全部给出).

(1)写出下列物质的化学式,A
(2)反应I中还原剂与氧化剂的物质的量之比为
反应Ⅱ的离子方程式为
反应Ⅲ的化学方程式为
(3)某人设想用如图所示装置用电化学原理生产E,N电极是

(4)当图中的C与O2被活性炭吸附时,也能发生放热反应生成D,为研究此反应,将C和O2放入体积为1L的恒容密闭容器中,在
500℃时发生反应,反应物浓度时间的变化如下表所示:
①反应从起始至2min内的平均反应速率v(C)=
②第6min时,向容器中再充入0.002molO2,同时将反应体系的温度改变为T,反应至10min时重新达到平衡,此时测得c(C)=
0.004mol/L,则温度T
查看习题详情和答案>>

(1)写出下列物质的化学式,A
Cu2S
Cu2S
,BCu2O
Cu2O
,HCu(OH)2
Cu(OH)2
.(2)反应I中还原剂与氧化剂的物质的量之比为
2:3
2:3
,反应Ⅱ的离子方程式为
Cu2O+2H+=Cu+Cu2++H2O
Cu2O+2H+=Cu+Cu2++H2O
.反应Ⅲ的化学方程式为
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(3)某人设想用如图所示装置用电化学原理生产E,N电极是
正
正
极;写出M电极的电极反应式:SO2+2H2O-2e-=SO42-+4H+
SO2+2H2O-2e-=SO42-+4H+
.
(4)当图中的C与O2被活性炭吸附时,也能发生放热反应生成D,为研究此反应,将C和O2放入体积为1L的恒容密闭容器中,在
500℃时发生反应,反应物浓度时间的变化如下表所示:
t(min) 浓度(mol/L) |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(C) | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
0.018mol/(L?min)
0.018mol/(L?min)
;500℃时,此反应化学平衡常数K的值为8000
8000
.②第6min时,向容器中再充入0.002molO2,同时将反应体系的温度改变为T,反应至10min时重新达到平衡,此时测得c(C)=
0.004mol/L,则温度T
<
<
(填“>”或“<”)500℃.化合物A由两种常见元素组成,且A中两种元素的质量比为4:1.A有如图所示转化关系,其中B、F均为红色固体,C能使品红溶液褪色(有的反应可能在水溶液中进行,有的反应的生成物未全部给出).
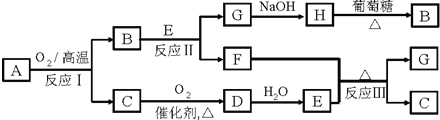
(1)写出下列物质的化学式,A______,B______,H______.
(2)反应I中还原剂与氧化剂的物质的量之比为______,
反应Ⅱ的离子方程式为______.
反应Ⅲ的化学方程式为______.
(3)某人设想用如图所示装置用电化学原理生产E,N电极是______极;写出M电极的电极反应式:______.
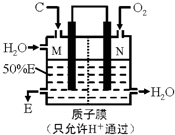
(4)当图中的C与O2被活性炭吸附时,也能发生放热反应生成D,为研究此反应,将C和O2放入体积为1L的恒容密闭容器中,在
500℃时发生反应,反应物浓度时间的变化如下表所示:
t(min) 浓度(mol/L) | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(C) | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
②第6min时,向容器中再充入0.002molO2,同时将反应体系的温度改变为T,反应至10min时重新达到平衡,此时测得c(C)=
0.004mol/L,则温度T______(填“>”或“<”)500℃. 查看习题详情和答案>>
化合物A由两种常见元素组成,且A中两种元素的质量比为4:1.A有如图所示转化关系,其中B、F均为红色固体,C能使品红溶液褪色(有的反应可能在水溶液中进行,有的反应的生成物未全部给出).
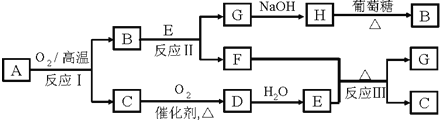
(1)写出下列物质的化学式,A______,B______,H______.
(2)反应I中还原剂与氧化剂的物质的量之比为______,
反应Ⅱ的离子方程式为______.
反应Ⅲ的化学方程式为______.
(3)某人设想用如图所示装置用电化学原理生产E,N电极是______极;写出M电极的电极反应式:______.
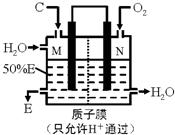
(4)当图中的C与O2被活性炭吸附时,也能发生放热反应生成D,为研究此反应,将C和O2放入体积为1L的恒容密闭容器中,在
500℃时发生反应,反应物浓度时间的变化如下表所示:
①反应从起始至2min内的平均反应速率v(C)=______;500℃时,此反应化学平衡常数K的值为______.
②第6min时,向容器中再充入0.002molO2,同时将反应体系的温度改变为T,反应至10min时重新达到平衡,此时测得c(C)=
0.004mol/L,则温度T______(填“>”或“<”)500℃.
查看习题详情和答案>>

(1)写出下列物质的化学式,A______,B______,H______.
(2)反应I中还原剂与氧化剂的物质的量之比为______,
反应Ⅱ的离子方程式为______.
反应Ⅲ的化学方程式为______.
(3)某人设想用如图所示装置用电化学原理生产E,N电极是______极;写出M电极的电极反应式:______.

(4)当图中的C与O2被活性炭吸附时,也能发生放热反应生成D,为研究此反应,将C和O2放入体积为1L的恒容密闭容器中,在
500℃时发生反应,反应物浓度时间的变化如下表所示:
t(min) 浓度(mol/L) |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(C) | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
②第6min时,向容器中再充入0.002molO2,同时将反应体系的温度改变为T,反应至10min时重新达到平衡,此时测得c(C)=
0.004mol/L,则温度T______(填“>”或“<”)500℃.
下图中,A、G是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,D、F、M为单质,I、L是正四面体结构的非极性分子,I是一种重要的能源,产物J是含B金属元素的胶状白色沉淀,K是由含B、D两种元素组成的化合物,N是淡黄色固体(图中部分反应物或生成物没有列出).
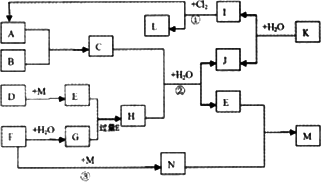
请按要求回答:
(1)元素B在元素周期表中的位置是________(填第几周期第几族).写出K的化学式________,L的电子式________.
(2)反应①进行的条件是________.
(3)反应②的离子方程式为________.
(4)反应③的化学方程式为________.
(5)写出Si与G溶液反应的离子方程式________.