网址:http://m.1010jiajiao.com/timu_id_1731713[举报]

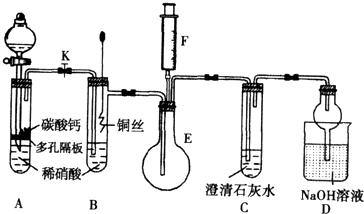
Ⅰ.(1)实验开始时先打开活塞K持续通入N2一段时间后,并闭K。将铜丝(足量)下移伸入浓硝酸后,有大量的红棕色气体生成,随时间的进行,气体颜色逐渐变浅,当A中充满无色气体时:
①装置A中反应的离子方程式为___________________________。
②接下来的实验操作是___________________________________。
(2)本实验中装置A的优点是____________________________。
Ⅱ.将B中所得溶液稀释至200 mL,用0.20 mol/L的NaOH溶液进行滴定。实验数据如下(硝酸的挥发分解及溶液体积的变化忽略不计):
实验编号 | 待测液体积(mL) | NaOH溶液体积(mL) |
1 | 20.00 | 15.98 |
2 | 20.00 | 14.99 |
3 | 20.00 | 15.01 |
(1)待测液的浓度为____________mol/L。
(2)硝酸与铜反应主要生成NO时硝酸的浓度不大于____________mol/L。
查看习题详情和答案>>
请回答有关问题:
(1)设计装置A的目的是
(2)当完成装置A的实验目的后,关闭K,再将装置B中的铜丝插入稀硝酸.B中反应的离子方程式是
(3)将F中的空气推入E中,证明NO存在的实验现象是
(4)装置D中NaOH溶液的作用是
某校课外活动小组为探究铜与稀硝酸反应产生的气体主要是NO,设计了下列实验。图中K为止水夹,F是装有一半空气的注射器,其中加热装置和固定装置均已略去。

请回答有关问题:
(1)设计装置A的目的是_______________________。
(2)当完成装置A的实验目的后,关闭K,再将装置B中的铜丝插入稀硝酸。B中反应的离子方程式是____________________________。
(3)将F中的空气推入E中,证明NO存在的实验现象是_______________,此过程发生反应的化学方程式是____________________。
(4)装置D中 溶液的作用是________________。
溶液的作用是________________。
查看习题详情和答案>>
某校课外活动小组为探究铜与稀硝酸反应产生的气体主要是NO,设计了下列实验。图中K为止水夹,F是装有一半空气的注射器,其中加热装置和固定装置均已略去。
请回答有关问题:
(1)设计装置A的目的是_______________________。
(2)当完成装置A的实验目的后,关闭K,再将装置B中的铜丝插入稀硝酸。B中反应的离子方程式是____________________________。
(3)将F中的空气推入E中,证明NO存在的实验现象是_______________,此过程发生反应的化学方程式是____________________。
(4)装置D中 溶液的作用是________________。
溶液的作用是________________。