摘要:15.为测定人体血液中Ca2+的含量.设计了如下方案: 有关反应的化学方程式为: 2KMnO4+5H2C2O4+3H2SO4 K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL.滴定生成的草酸消耗0.001mol·L-1的KMnO4溶液15.0mL.则这种血液样品中的含钙量为 ( ) A.0.001mol·L-1 B.0.0025mol·L-1 C.0.0003mol·L-1 D.0.0035mol·L-1 第Ⅱ卷(必做120分+选做32分.共152分) 20080428 20080428 注意事项:
网址:http://m.1010jiajiao.com/timu_id_1731201[举报]
为测定人体血液中Ca2+的含量,设计了如下方案:
有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗了0.001mol?L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为( )

有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗了0.001mol?L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为( )
查看习题详情和答案>>
为测定人体血液中Ca2+的含量,设计了如下方案:

有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗了0.001mol?L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为( )
查看习题详情和答案>>

有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗了0.001mol?L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为( )
| A.0.001mol?L-1 | B.0.0025mol?L-1 |
| C.0.0003mol?L-1 | D.0.0035mol?L-1 |
为测定人体血液中Ca2+的含量,设计了如下方案:
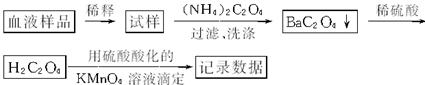
有关反应的化学方程式为:
2KMnO4+5H![]() K2SO4+2MnSO4+10CO2↑+8H2O,若血液样品为15 mL,滴定生成的草酸消耗0.001 mol·L-1的KMnO4溶液15.0 mL,则这种血液样品中的含钙量为
K2SO4+2MnSO4+10CO2↑+8H2O,若血液样品为15 mL,滴定生成的草酸消耗0.001 mol·L-1的KMnO4溶液15.0 mL,则这种血液样品中的含钙量为
C.0.000 3 mol·L-1 D.0.003 5 mol·L-1
查看习题详情和答案>>
