题目内容
为测定人体血液中Ca2+的含量,设计了如下方案: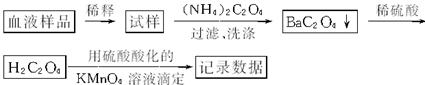
有关反应的化学方程式为:
2KMnO4+5H![]() K2SO4+2MnSO4+10CO2↑+8H2O,若血液样品为15 mL,滴定生成的草酸消耗0.001 mol·L-1的KMnO4溶液15.0 mL,则这种血液样品中的含钙量为
K2SO4+2MnSO4+10CO2↑+8H2O,若血液样品为15 mL,滴定生成的草酸消耗0.001 mol·L-1的KMnO4溶液15.0 mL,则这种血液样品中的含钙量为
C.0.000 3 mol·L-1 D.0.003 5 mol·L-1
B 2KMnO4—5H
2 mol 5 mol
0.001 mol·L-1×
c(Ca2+)=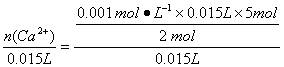 =0.002 5 mol·L-1,B正确。
=0.002 5 mol·L-1,B正确。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目




