摘要:3.第Ⅱ卷所有题目的答案考生须用0.5mm黑色签字笔答在答题纸规定位置上在试题卷上答题无效. [必做部分]
网址:http://m.1010jiajiao.com/timu_id_1731189[举报]
几种短周期元素的原子半径及某些化合价见下表:
分析上表中有关数据,并结合已学过的知识,回答以下问题.涉及上述元素的答案,请用元素符号表示.
(1)E元素在周期表中位于
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)A与J所形成化合物中的化学键类型是
 .
.
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
查看习题详情和答案>>
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +6、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
(1)E元素在周期表中位于
第三
第三
周期,ⅥA
ⅥA
族;(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
F-、Na+、Al3+
F-、Na+、Al3+
(3)A与J所形成化合物中的化学键类型是
离子键
离子键
,用电子式表示其形成过程

(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
.
8.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域,已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象( )
A.18O 31P 119Sn
B.27Al 19F 12C
C.元素周期表中ⅤA族所有元素的原子
D.元素周期表中第Ⅰ周期所有元素的原子
查看习题详情和答案>>(1)在粗制CuSO4?5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
A.NaOH B.NH3?H2O C.CuO D.Cu(OH)2
(3)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,设溶液中CuSO4的物质的量浓度为3.0mol?L-1,则Cu(OH)2开始沉淀时溶液的pH为
查看习题详情和答案>>
B
B
.A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
(2)然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
CD
CD
.A.NaOH B.NH3?H2O C.CuO D.Cu(OH)2
(3)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,设溶液中CuSO4的物质的量浓度为3.0mol?L-1,则Cu(OH)2开始沉淀时溶液的pH为
4
4
,完全沉淀时溶液的pH为6.7
6.7
,通过计算确定pH=4时,Fe3+残存的浓度是:8×10-8mol/L
8×10-8mol/L
.(请写出第3小题的计算过程.lg3=0.48)下表为部分短周期元素化合价及相应氢化物沸点的数据:
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;②B与D可形成化合物BD、BD2,可用于制备强酸乙.
请回答:
(1)表中属于第三周期元素的是
(2)写出H的最高价氧化物的电子式:
 ,比较A、D、G三种简单阴离子的半径大小:
,比较A、D、G三种简单阴离子的半径大小:
r(
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是:
(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:BD+BD2+Na2CO3=2
①横线上某盐的化学式应为
(6)请设计一个实验方案,使得铜和稀的强酸甲反应,得到蓝色溶液和氢气,在答题卡指定位置绘出实验装置图,标出必要的说明即可
 .
.
查看习题详情和答案>>
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
| 最高化合价 | +6 | +5 | +4 | +5 | +7 | +4 | ||
| 最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
请回答:
(1)表中属于第三周期元素的是
ACEG
ACEG
(用表中元素编号填写).(2)写出H的最高价氧化物的电子式:


r(
S2-
S2-
)>r(Cl-
Cl-
)>r(O2-
O2-
) (用元素符号表示)(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab
ab
.a.MnO2b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是:
SOCl2+H2O=SO2+2HCl
SOCl2+H2O=SO2+2HCl
.(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:BD+BD2+Na2CO3=2
NaNO2
NaNO2
+CO2①横线上某盐的化学式应为
NaNO2
NaNO2
;②每产生44.8L(标准状况)CO2,被吸收尾气的质量是152
152
g.(6)请设计一个实验方案,使得铜和稀的强酸甲反应,得到蓝色溶液和氢气,在答题卡指定位置绘出实验装置图,标出必要的说明即可


工业制硝酸的主要反应是:4NH3(g)+5O2(g)?4NO(g)+6H2O (g)+1025kJ
(1)该反应的平衡常数表达式为K=
;升高温度K值
(2)若反应物起始的物质的量相同,如图所示关系图错误的是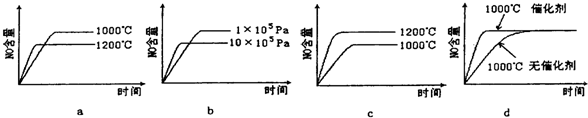
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①起始时物料比c(O2):c(NH3)>1.25,其原因是
②反应在第2min到第4min时O2的平均反应速率为
③反应在第2min改变了反应条件,改变的条件可能是
a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是
查看习题详情和答案>>
(1)该反应的平衡常数表达式为K=
| c4(NO)c6(H2O) |
| c4(NH3)c5(O2) |
| c4(NO)c6(H2O) |
| c4(NH3)c5(O2) |
减小
减小
(填“增大”、“减小”或“不变”).(2)若反应物起始的物质的量相同,如图所示关系图错误的是
c
c
(填字母序号).
(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 1.6 | 0.5 |
增大氨气的转化率
增大氨气的转化率
.②反应在第2min到第4min时O2的平均反应速率为
0.1875
0.1875
mol/L?min;③反应在第2min改变了反应条件,改变的条件可能是
c
c
(填字母序号).a.使用催化剂 b.升高温度 c.增大压强 d.增加O2的浓度
④反应在第8min改变的反应条件可能是
增大反应物的浓度.
增大反应物的浓度.
.