摘要:21.在稀硫酸溶液中.4.48gCu2S和CuS的混合物与100mL 0.75mol·L-1的MnO反应生成了SO.Cu2+和Mn2+.剩余的MnO恰好与35.0mL 1.00mol·L-1 FeSO4溶液反应. (1)配平下列反应化学方程式: Cu2S+ MnO+ H+ Cu2++ SO+ Mn2++ H2O (2)试计算原始混合物中Cu2S的质量分数.
网址:http://m.1010jiajiao.com/timu_id_1719363[举报]
(08杭州五校月考)在稀硫酸溶液中,4.48g Cu2S和CuS的混合物与100mL 0.75mol?L-1的MnO4-反应生成了SO42-、Cu2+和Mn2+。
剩余的MnO4-恰好与35.0mL 1.00mol?L-1 FeSO4溶液反应(还原产物Mn2+, 氧化产物Fe3+)。
(1)配平下列反应化学方程式:
____Cu2S+____ MnO4-+____H+===____ Cu2++____SO42-+____ Mn2+ +____H2O
____CuS+____ MnO4-+____H+===____ Cu2++____SO42-+____ Mn2+ +____H2O
(2)试计算原始混合物中Cu2S的质量分数。
查看习题详情和答案>>
在稀硫酸溶液中,4.48 g Cu2S和CuS的混合物与100 mL 0.75 mol·L-1的 反应生成了
反应生成了 、Cu2+和Mn2+。剩余的
、Cu2+和Mn2+。剩余的 恰好与35.0 mL 1.00 mol·L-1FeSO4溶液反应。
恰好与35.0 mL 1.00 mol·L-1FeSO4溶液反应。
(1)配平下列反应化学方程式:
____Cu2S+____![]() +____H+
+____H+![]() _____Cu2+_____+
_____Cu2+_____+![]() +_____Mn2++_____H2O
+_____Mn2++_____H2O
(2)试计算原始混合物中Cu2S的质量分数。
查看习题详情和答案>>已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.室温下元素W的单质是淡黄色粉末状固体,在空气中燃烧生成的气体是形成酸雨的主要污染物之一.元素R的单质在常温常压下是黄绿色气体,能溶于水.请回答下列问题:
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价电子的轨道表示式为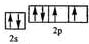
 ,该元素的名称是
,该元素的名称是
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
(5)W、R 两元素非金属性较强的是
查看习题详情和答案>>
(1)X元素原子基态时的电子排布式为
1s22s22p63s23p63d104s24p3
1s22s22p63s23p63d104s24p3
,该元素的符号是As
As
;(2)Y元素原子的价电子的轨道表示式为


氧
氧
;(3)X与Z可形成化合物XZ3,该化合物的空间构型为
三角锥
三角锥
;(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
;(5)W、R 两元素非金属性较强的是
Cl
Cl
(写元素符号).写出能够证明这一结论的一个实验事实高氯酸的酸性强于硫酸或氯化氢的稳定性强于硫化氢
高氯酸的酸性强于硫酸或氯化氢的稳定性强于硫化氢
.(2009?辽宁)[化学-选修物质结构与性质]
已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价层电子的轨道表示式为
 ,该元素的名称是
,该元素的名称是
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
(5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由
查看习题详情和答案>>
已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.请回答下列问题:
(1)X元素原子基态时的电子排布式为
1s22s22p63s23p63d104s24p3
1s22s22p63s23p63d104s24p3
,该元素的符号是As
As
;(2)Y元素原子的价层电子的轨道表示式为


氧
氧
;(3)X与Z可形成化合物XZ3,该化合物的空间构型为
三角锥
三角锥
;(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
;(5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由
稳定性:NH3>PH3>AsH3因为键长越短,键能越大,化合物越稳定;沸点:NH3>AsH3>PH3;NH3可形成分子间氢键,沸点最高,AsH3相对分子质量比PH3大,分子间作用力大,因而AsH3比PH3沸点高
稳定性:NH3>PH3>AsH3因为键长越短,键能越大,化合物越稳定;沸点:NH3>AsH3>PH3;NH3可形成分子间氢键,沸点最高,AsH3相对分子质量比PH3大,分子间作用力大,因而AsH3比PH3沸点高
.已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子.X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子.
请回答下列问题:
(1)X元素原子基态时的电子排布式为
(2)Y元素原子的价层电子的轨道表示式为
 ,该元素的名称是
,该元素的名称是
(3)X与Z可形成化合物XZ3,该化合物的空间构型为
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
(5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性高低
查看习题详情和答案>>
请回答下列问题:
(1)X元素原子基态时的电子排布式为
1s22s22p63s23p63d104s24p3
1s22s22p63s23p63d104s24p3
,该元素的符号是As
As
.(2)Y元素原子的价层电子的轨道表示式为


氧
氧
.(3)X与Z可形成化合物XZ3,该化合物的空间构型为
三角锥
三角锥
.(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
三角锥
三角锥
.(5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性高低
稳定性:NH3>PH3>AsH3
稳定性:NH3>PH3>AsH3
,理由是因为键长越短,键能越大,化合物越稳定
因为键长越短,键能越大,化合物越稳定
.