网址:http://m.1010jiajiao.com/timu3_id_80419[举报]
(2)标准状况下,2mol NH3与
(3)等质量的O2和O3所含的原子个数之比是
(4)实验室使用的浓盐酸的溶质的质量分数一般为36.5%,密度为1.19g/cm-3,将
无机化合物在化工生产和科学研究中发挥着重要的作用.根据题意完成下列计算:
1.一定温度下,将60 mL CO、CO2与O2的混合气体用电火花引燃,完全反应后冷却到原来温度,体积减少了10 mL.将反应后的气体通过足量的NaOH(aq),体积又减少了30 mL.剩余气体可使带余烬的木条复燃.原混合气中CO的体积为________mL,CO2的体积为________mL.
2.标准状况下CO与CO2混合气体的平均相对分子质量为32.将该气体完全通入盛有足量Na2O2的容积为2.24升的密闭容器中(忽略固体物质的体积),引燃,完全反应后,容器内固体生成物的质量为________g.
3.将Fe2O3溶于150 mL稀H2SO4中,待Fe2O3完全溶解后,加入铁粉,产生气体3.36 L(标准状况),溶液中不再有Fe和Fe3+.已知加入的铁粉和氧化铁共19.2 g,计算:
(1)Fe2O3的质量为________g;
(2)稀H2SO4物质的量浓度为________.
4.取5.64 g Cu(NO3)2无水晶体,强热使其分解,得到NO2、O2和2.32固体氧化物.将气体用水充分吸收后,还有气体剩余,同时得到100 mL溶液.请通过计算确定:(写出计算过程)
(1)所得溶液的物质的量浓度;
(2)残留固体的成分和质量分别是多少克?
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中________________能导致酸雨的形成;目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化。
如:CO(g)+NO2(g)![]() NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
据此回答:若用标准状况下
(2)在火力发电厂产生的废气中含有SO2、N2、CO等气体,为除去SO2,常用Ca(OH)2悬浊液洗涤废气,为了废物利用,再通入空气使反应产物转化为石膏(CaSO4·2H2O)。写出有关的化学反应方程式______________。
(3)硫酸工业生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196 kJ·mol-1
2SO3(g) ΔH=-196 kJ·mol-1

某温度下达到平衡时,SO2的体积百分含量与体系的总压强的关系如上图所示:
据此图回答下列问题:
①平衡状态由A变到B时,反应体系____________(填“吸收”或“释放”)能量。
②将5 mol SO2和7 mol O2通入

(1)X与A溶液反应的离子方程式为
(2)把红热的木炭投入到L的浓溶液中,可发生剧烈反应,①化学方程式为
| ||
| ||
②若把产生的气体通入足量的饱和碳酸氢钠溶液中,再把逸出的气体干燥后通入足量的过氧化钠固体,充分反应后,再通入水中,最后收集到的气体是
③若把产生的气体直接通入足量的澄清石灰水中,现象是
(3)将K、I、G混合气体充满容器后倒置于水槽中,气体完全溶解,溶液充满整个容器.则三者的物质的量之比可能为
A.1:1:1 B.4:2:2.5 C.4:8:7 D.6:4:5
所得溶液的浓度范围
(4)熔融条件下,化合物A中金属元素所对应的单质Z与Q可组成可充电电池(装置如下),

反应原理为:2Z+Q
| 放电 |
| 充电 |
①放电时,电池的正极反应式为
②充电时,
(13分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CH3OH)= 0.8 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
④恒温、恒容时,下列情况不能说明反应I已经达到化学平衡状态的是________________。
 a、容器各物质的浓度保持不变; b、容器内压强保持不变;
a、容器各物质的浓度保持不变; b、容器内压强保持不变; c、υ(CO)消耗==1/2υ(H2)生成 d 、容器内的密度保持不变
c、υ(CO)消耗==1/2υ(H2)生成 d 、容器内的密度保持不变(2)25℃、101kPa时,燃烧16g液体甲醇生成CO2和H2O(l),放出的热量为363.26kJ,写出甲醇燃烧的热化学方程式: 。
(3)某实验小组依据甲醇燃烧的反应原理,设计一个燃料电池电解Na2SO4溶液(图如下)。请根据图示回答下列问题:
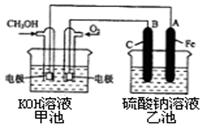
①通入甲醇蒸气的电极应为 极(填写“正”或“负”), 该电极上发生的电极反应是 (填字母代号)。
a.2CH3OH —12 e- +3O2 === 2CO2 + 4 H2O
b.CH3OH—6 e- + 8 OH- ="==" CO32- + 6H2O
c.O2 + 2H2O + 4 e- ="==" 4OH-
d.O2— 4 e- + 4H+ ="==" 2H2O
②写出电极A的名称 。写出B电极的电极反应式 。
③当酸性甲醇燃料电池消耗3.36 L 氧气时(折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是 。 查看习题详情和答案>>