摘要: (1)大部分原子半径是 米,工厂合成氨采用的压强是 帕. (2)与Pb2+具有相同电子层结构的稳定阳离子有 和 . (3)乙炔与水发生加成反应后的主要产物是 .2-丁炔与水发生加成反应后的主要产物是 .
网址:http://m.1010jiajiao.com/timu3_id_435054[举报]
前四周期元素A、B、C、D、E,原子序数依次增大.已知:A、C同主族,A的原子最外层电子数是次外层的3倍,B的氧化物既能溶于强酸,又能溶于强碱,D的原子半径是第三周期中最小的,E是形成骨骼和牙齿的主要元素,且E单质能和水反应.则下列分析错误的是( )
查看习题详情和答案>>
现有A、B、C、D、E、F六种常见的短周期元素,原子序数依次递增,A的原子半径是所有元素中最小的,B、C、D为第2周期相邻的三种元素,且原子半径B>C>D,F是第3周期元素,最外层电子数为6,C和F同主族,E和A同主族.请回答:
(1)写出元素A在元素周期表中的位置 ;
(2)C与E可形成离子化合物E2C,试写出它的电子式 ;
(3)B的最高价氧化物的水化物能与B的氢化物反应生成盐类物质,其化学反应方程式: ;
(4)F的低价氧化物与C的某一种氢化物发生氧化还原反应,其化学反应方程式: ;
(5)D与F的单质一定条件下反应生成FD6.该物质是一种人工合成的惰性气体,曾用于曼哈顿核计划,现广泛应用于电力工业.则当FD6形成晶体时,其晶体类型为 ;
(6)在1L的密闭容器中,通入1mol B2气体和3mol A2气体,一定温度下反应生成BA3气体,当反应达到平衡时,B2的浓度为0.75mol.L-1,同时放出约23.1kJ的热量,该反应的热化学方程式是 .
查看习题详情和答案>>
(1)写出元素A在元素周期表中的位置
(2)C与E可形成离子化合物E2C,试写出它的电子式
(3)B的最高价氧化物的水化物能与B的氢化物反应生成盐类物质,其化学反应方程式:
(4)F的低价氧化物与C的某一种氢化物发生氧化还原反应,其化学反应方程式:
(5)D与F的单质一定条件下反应生成FD6.该物质是一种人工合成的惰性气体,曾用于曼哈顿核计划,现广泛应用于电力工业.则当FD6形成晶体时,其晶体类型为
(6)在1L的密闭容器中,通入1mol B2气体和3mol A2气体,一定温度下反应生成BA3气体,当反应达到平衡时,B2的浓度为0.75mol.L-1,同时放出约23.1kJ的热量,该反应的热化学方程式是
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子,B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E主族.
(1)B在周期表中的位置第
(2)E元素形成的氧化物对应的水化物的化学式为
(3)元素C、D、E形成的离子半径大小关系是
(4)用电子式表示化合物D2C的形成过程
 .C、D还可形成化合物D2C2,D2C2含有的化学键是
.C、D还可形成化合物D2C2,D2C2含有的化学键是
(5)由A、B、C三种元素形成的离子化合物的化学式为
(6)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为(化学式用具体的元素符号表示):
查看习题详情和答案>>
(1)B在周期表中的位置第
二
二
周期,第VA
VA
族;(2)E元素形成的氧化物对应的水化物的化学式为
H2SO3、H2SO4
H2SO3、H2SO4
;(3)元素C、D、E形成的离子半径大小关系是
S2-
S2-
>O2-
O2-
>Na+
Na+
(用离子符号表示).(4)用电子式表示化合物D2C的形成过程


离子键、非极性共价键(或离子键、共价键)
离子键、非极性共价键(或离子键、共价键)
.(5)由A、B、C三种元素形成的离子化合物的化学式为
NH4NO3
NH4NO3
,它与强碱溶液反应的离子方程式是NH4++OH-=NH3?H2O
NH4++OH-=NH3?H2O
.(6)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为(化学式用具体的元素符号表示):
4Na2SO3=Na2S+3Na2SO4
4Na2SO3=Na2S+3Na2SO4
.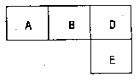 有M、A、B、D、E五种短周期元素,其原子序数依次增大,M元素的原子半径是周期表所有元素中最小的.A、B、D、E分别在下表中(周期表的一部分)不同的空格内占有相应的位置,它们的原子序数之和为37.请回答:
有M、A、B、D、E五种短周期元素,其原子序数依次增大,M元素的原子半径是周期表所有元素中最小的.A、B、D、E分别在下表中(周期表的一部分)不同的空格内占有相应的位置,它们的原子序数之和为37.请回答:(1)元素符号:A
(2)D、E两种元素分别与M元素形成的最简单化合物中,相对稳定的是
(3)A、B、D、M可组成多种18电子的分子,其中的两种结构可分别表示为M2B-BM2和AM3-BM2,请再写出2种具有18电子的有机物的结构简式
(4)M、B、D以原子个数比4:2:3所形成的离子化合物,其水溶液呈
 已知短周期元素X、Y、Z的原子序数依次增大,且Z的原子序数等于X和Y的原子序数之和,Y的原子半径是同同期元素中最小的,Z元素在地壳中的含量居第二位.根据以上叙述下列说法中正确的是( )
已知短周期元素X、Y、Z的原子序数依次增大,且Z的原子序数等于X和Y的原子序数之和,Y的原子半径是同同期元素中最小的,Z元素在地壳中的含量居第二位.根据以上叙述下列说法中正确的是( )