网址:http://m.1010jiajiao.com/timu3_id_420349[举报]
下表中所列的是六种短周期元素原子的半径及主要化合价:
| 元素代号 | A | B | C | D | E | G |
| 原子半径/nm | 0.089 | 0.071 | 0.117 | 0.16 | 0.074 | 0.082 |
| 主要化合价 | +2 | -1 | +4,-4 | +2 | -2 | +3 |
(1)C元素在周期表中的位置为 ;E原子的电子填充在 个轨道上,这些电子有 种不同的能量。
(2)B、D、E所代表元素的离子半径从大到小的顺序为 (填离子符号)。
(3)C与E形成的化合物属于 晶体。
(4)周期表中有些元素存在“对角线相似”现象(一种元素的性质常同它右下方相邻的另一种元素具有类似性),请写出A的单质与强碱溶液反应的离子方程式: 。
(5)已知X是与E同族的另一短周期元素,有人认为:H—E键的键能大于H—X键的键能,所以H2E的沸点高于H2X的沸点。你是否赞同这种观点 (填“赞同”或“不赞同”),理由: 。
查看习题详情和答案>>
下表中所列的是六种短周期元素原子的半径及主要化合价:
|
元素代号 |
A |
B |
C |
D |
E |
G |
|
原子半径/nm |
0.089 |
0.071 |
0.117 |
0.16 |
0.074 |
0.082 |
|
主要化合价 |
+2 |
-1 |
+4,-4 |
+2 |
-2 |
+3 |
(1)C元素在周期表中的位置为 ;E原子的电子填充在 个轨道上,这些电子有 种不同的能量。
(2)B、D、E所代表元素的离子半径从大到小的顺序为 (填离子符号)。
(3)C与E形成的化合物属于 晶体。
(4)周期表中有些元素存在“对角线相似”现象(一种元素的性质常同它右下方相邻的另一种元素具有类似性),请写出A的单质与强碱溶液反应的离子方程式: 。
(5)已知X是与E同族的另一短周期元素,有人认为:H—E键的键能大于H—X键的键能,所以H2E的沸点高于H2X的沸点。你是否赞同这种观点 (填“赞同”或“不赞同”),理由: 。
查看习题详情和答案>>
①原子半径大小:A>B>C>D
②A、B、C、D四种元素之间形成的甲、乙、丙三种分子的比例模型及部分性质:
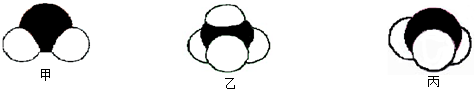
甲:所有生命体生存依赖的重要资源,约占人体体重的三分之二.
乙:无色,无味、易燃气体,是常见的一种化石燃料.
丙:极易溶于水、有刺激性气味气体,其溶液能使红色石蕊试纸变蓝.
③E的金属性最强,F的单质在常温下可以被B的含氧酸钝化.
请根据上述信息回答下列问题.
(1)A元素在周期表中的位置
(2)由A、B、C、D中元素形成的两种离子,反应能生成丙,其离子方程式为
(3)E、F两元素的最高价氧化物的水化物之间反应的离子方程式为
(4)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有硫酸亚铁溶液(硫酸酸化)的试管中,逐滴滴加丁溶液,观察到溶液由浅绿色变成黄色,其反应的离子方程式
 短周期元素A-F的原子序数依次增大,部分元素的信息如下:
短周期元素A-F的原子序数依次增大,部分元素的信息如下:| 元素编号 | 信息 |
| B | 与元素A、D共同组成的化合物的种类最多 |
| D | 最外层电子数是次外层电子数的三倍 |
| E | 同周期元素中形成的简单离子半径最小 |
| F | 最高价氧化物对应的水化物的酸性最强 |
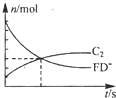
(1)某容器中发生一个化学反应,反应过程中存在A2D、FD-、BC-,ABD3-、C2、F-等六种粒子,测得FD-和C2的物质的量随时间变 化的曲线如图所示.请写出该反应的离子方程式
(2)W与D是相邻的同主族元素.在下表中列出H2WO3的不同化学性质,举例并写出 相应的化学方程式
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3=3H3PO4+H2W↑ |
| ① | ||
| ② |
①写出甲的溶液与乙的溶液反应的离子方程式
②鉴定丁中阳离子的操作是
③如果丁中含有元素F,丁的溶液中离子浓度由大到小的排列顺序是
现有六种短周期元素A、B、C、D、E、F,其原子序数依次增大,其中B与C、D与F分别位于同一周期,A与D、C与F分别位于同一主族,且A、D两元素原子的质子数之和是C、F两元素原子质子数之和的一半。又知六种元素所形成的常见单质在常温常压下三种是气体,;种是固体。请回答下列问题:
(1)B元素单质的电子式 ,F元素氧化物的晶体类型为 。
(2)由A、C两元素可组成X、Y两种化合物,X在MnO2作用下可以分解成Y,写出X转化为Y的化学方程式 。
(3)若E是非金属元素,但能表现出一些金属元素的性质。写出E与D的氧化物的水溶液反应的离子方程式 。
(4)一定条件下,A的单质与B的单质充分反应生成6.8gW气体时,可放出18.48kJ热量,写出该反应的热化学方程式 。
查看习题详情和答案>>