摘要:25.★配制1L含氨质量分数为10%的氨水.按下列两种计算方法.求出需要氨气在标准状况下的体积(升): (1)按气体摩尔体积求解: (2)按密度求解(标准状况下氨气的密度为0.771克/升): (3)经比较知.你认为第 种更准确.理由是 .
网址:http://m.1010jiajiao.com/timu3_id_341267[举报]
在无土栽培中,需配制1L含0.50mol?L-1的NH4Cl、0.16mol?L-1KCl、0.24mol?L-1K2SO4的混合溶液,但当时没有K2SO4固体,若用(NH4)2SO4固体代替,需用KCl、NH4Cl、(NH4)2SO4三种固体的物质的量(单位为 mol)分别为( )
查看习题详情和答案>>
在无土裁培中,配制1L含0.5mol NH4Cl、0.16mol KCl、0.24mol K2SO4的某营养液,若用KCl、NH4Cl和(NH4)2SO4三种固体配制,则需此三种固体的物质的量分别为( )
查看习题详情和答案>>
琉酸是无机“三大强酸"之一,其产量是衡量一个国家无机化工发展水平的重要标志。工业制硫酸的工艺流程如下图:

据图回答下列问题:
(1)写出用黄铁矿(主要含FeS2)造气的化学反应方程式________。
(2) 给出A、B物质的名称:A________, B________
(3) 催化氧化之前对SO2和空气的混合气体进行净化、干燥的目的是________ 选用B进入吸收塔吸收SO3的优点是________。
(4) SO2的催化氧化是一个可逆反应,采取适宜的反应条件有利于生产的进行。实际生产中,下列哪些生产条件或措施考虑到了平衡移动原理________ (选填序号)。
A.矿石加入沸腾炉之前先粉碎
B.使用V2O5作催化剂
C.催化反应室中选择400-5000C温度
D.净化后的炉气中要有过量的空气
E. 催化氧化在常压下进行
F. 将尾气中的SO2循环利用
(5) 某硫酸厂每天消耗黄铁矿石(含FeS2质量分動60%) 20吨,生产的三阶段的转化率依次为98%、95%、98%,则该工厂一天能生产B的质量为__________吨。
查看习题详情和答案>>
实验室要配制1L含0.17molK2SO4、0.16molKCl、0.50molNaCl的溶液.现因无K2SO4,只有Na2SO4、KCl、NaCl,如何配制所需溶液?简述操作步骤.
查看习题详情和答案>>明矾石的主要成分是K2SO4?Al2(SO4)3?2Al2O3?6H2O,此外还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下:
明矾石脱水废渣调节pH溶液硫磺焙烧溶解氢氧化钠氢氧化铝母液 硫酸炉气熟料
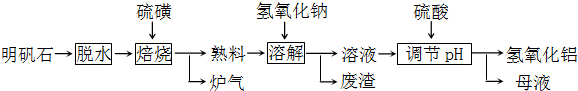
回答下列问题:
(1)“焙烧”过程中发生的反应为2Al2(SO4)3+3S
2Al2O3+9SO2,其中氧化剂为 .
(2)“溶解”时反应的离子方程式为 .
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是 .
(4)调节pH时使用的是质量浓度(单位体积溶液所含溶质的质量)为882g/L 的H2SO4,配制1L该溶液,需用量筒量取质量分数为98%的硫酸(密度是1.8g/cm3) mL
(5)“废渣”、“母液”中可回收的物质分别是 .
查看习题详情和答案>>
明矾石脱水废渣调节pH溶液硫磺焙烧溶解氢氧化钠氢氧化铝母液 硫酸炉气熟料

回答下列问题:
(1)“焙烧”过程中发生的反应为2Al2(SO4)3+3S
| ||
(2)“溶解”时反应的离子方程式为
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是
(4)调节pH时使用的是质量浓度(单位体积溶液所含溶质的质量)为882g/L 的H2SO4,配制1L该溶液,需用量筒量取质量分数为98%的硫酸(密度是1.8g/cm3)
(5)“废渣”、“母液”中可回收的物质分别是