摘要:解:50千克硫酸铵样品中含(NH4)2SO4的质量为: 50千克×95% = 47.5千克 (NH4)2SO4中N元素的质量分数为: 则:硫酸铵样品中含氮元素的质量为:
网址:http://m.1010jiajiao.com/timu3_id_328805[举报]
(2010?潮州二模)过氧化氢是重要的氧化剂、还原剂,其水溶液又称双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定过氧化氢的含量,并探究过氧化氢的性质、用途.
Ⅰ.测定过氧化氢的含量
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL 容量瓶中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
.
(3)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
Ⅱ.探究过氧化氢的性质
(4)该化学兴趣小组根据所提供的实验条件设计了两个实验,分别验证过氧化氢的氧化性和不稳定性.(实验试剂只有:过氧化氢溶液、稀硫酸、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)请填写他们的实验方法和实验现象的表中空白:
Ⅲ.用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜
(5)印刷电路板金属粉末中的Cu在H2SO4与H2O2溶液中反应生成Cu2+和H2O的离子方程式为
(6)控制其他条件相同,印刷电路板的Cu用10%H2O2和3.0mol/L H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率如下表:
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是
查看习题详情和答案>>
Ⅰ.测定过氧化氢的含量
(1)移取10.00mL密度为ρ g/mL的过氧化氢溶液至250mL 容量瓶中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下:2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
| 17Cv |
| 200ρ |
| 17Cv |
| 200ρ |
(3)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
偏高
偏高
(填“偏高”或“偏低”或“不变”).Ⅱ.探究过氧化氢的性质
(4)该化学兴趣小组根据所提供的实验条件设计了两个实验,分别验证过氧化氢的氧化性和不稳定性.(实验试剂只有:过氧化氢溶液、稀硫酸、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选.)请填写他们的实验方法和实验现象的表中空白:
| 实验内容 | 实验方法 | 实验现象 |
| 验证氧化性 | 取适量碘化钾淀粉溶液、稀硫酸于试管中,滴入过氧化氢溶液.(或:取适量饱和硫化氢溶液于试管中,滴入过氧化氢溶液.) | 溶液变蓝色 溶液变蓝色 .(或: 产生淡黄色沉淀或溶液变浑浊 产生淡黄色沉淀或溶液变浑浊 ) |
| 验证热不稳定性 | 取适量过氧化氢溶液于试管中, 稍微加热 稍微加热 用带火星的木条检验 用带火星的木条检验 . |
产生气泡,带火星的木条复燃. |
(5)印刷电路板金属粉末中的Cu在H2SO4与H2O2溶液中反应生成Cu2+和H2O的离子方程式为
Cu+H2O2+2H+=Cu2++2H2O
Cu+H2O2+2H+=Cu2++2H2O
.(6)控制其他条件相同,印刷电路板的Cu用10%H2O2和3.0mol/L H2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率 (×10-3mol?L-1?min-1) |
7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
温度升高,H2O2分解速率加快
温度升高,H2O2分解速率加快
.
亚硫酸钠用途广泛,可作漂白剂、显影剂、防护剂等.近年来,以SO2、NH3和NaCl为原料生产无水亚硫酸钠的新方法得到发展.生产流程如图1所示:
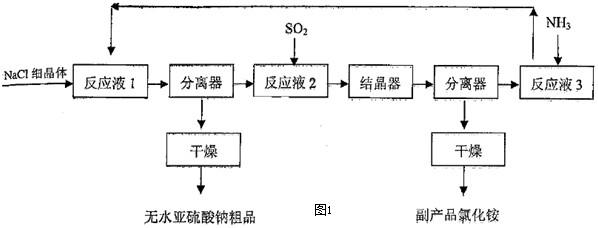
(1)中学化学实验室实现上述流程中“分离器”作用的操作名称是: ;所需玻璃仪器有 .
(2)“反应液1”是由SO2通入14.8%氨水形成的亚硫酸铵溶液,在60℃~80℃时,不断搅拌,加入NaCl细晶体,就有无水亚硫酸钠析出,析出无水亚硫酸钠的离子反应方程式为 .
(3)在“反应液2”通入足量SO2后,溶液中的阴离子除OH-外还有 ;在“反应液3”中通入足量NH3的目的是: .
(4)该生产方法的原料利用率(每制100g无水亚硫酸钠,各物质的消耗量及副产品物量)如表格:
副产品NH4Cl的理论值a为: ;它与NH4Cl实际值有差别的可能原因是: .
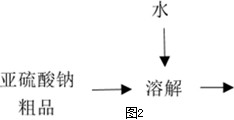
(5)无水亚硫酸钠粗品常用重结晶的方法进行精制,请完善能实现物料循环的精制亚硫酸钠操作的流程图(如图2所示).
 查看习题详情和答案>>
查看习题详情和答案>>

(1)中学化学实验室实现上述流程中“分离器”作用的操作名称是:
(2)“反应液1”是由SO2通入14.8%氨水形成的亚硫酸铵溶液,在60℃~80℃时,不断搅拌,加入NaCl细晶体,就有无水亚硫酸钠析出,析出无水亚硫酸钠的离子反应方程式为
(3)在“反应液2”通入足量SO2后,溶液中的阴离子除OH-外还有
(4)该生产方法的原料利用率(每制100g无水亚硫酸钠,各物质的消耗量及副产品物量)如表格:
| 原料 | 理论值 | 实际值 | 利用率 |
| SO2 | 50.79 | 54.4 | 93.36% |
| NaCl | 92.86 | 101.0 | 91.94% |
| NH3 | 26.98 | 30.5 | 88.46% |
| 副产品NH4Cl | a | 87.1 | -------- |
(5)无水亚硫酸钠粗品常用重结晶的方法进行精制,请完善能实现物料循环的精制亚硫酸钠操作的流程图(如图2所示).
 查看习题详情和答案>>
查看习题详情和答案>>
通常状况下,过氧化氢是一种无色透明的液体,在实验室和生产中应用广泛.
(1)火箭推进器中分别装有联氨(N2H4)和过氧化氢,它们发生反应的热化学方程式为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-642.2kJ?mol-1
又知:2H2O2(l)=2H2O(l)+O2(g)△H=-196.4kJ?mol-1
H2O(l)=H2O(g)△H=44kJ?mol-1
请写出N2H4(l)与O2(g)反应生成N2(g)和H2O(l) 的热化学方程式: .
(2)H2O2是一种二元弱酸,其第一步电离的电离方程式为 .
(3)过二硫酸铵法是目前最流行的制备H2O2的方法.即电解含 H2SO4的(NH4)2SO4溶液制取(NH4)2S2O8,如图1所示,再加热水解即可得H2O2和(NH4)2SO4.
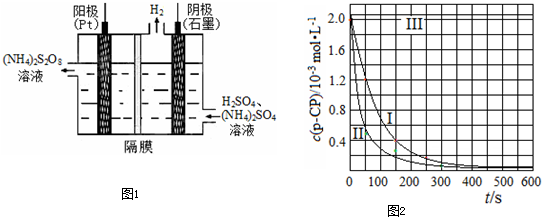
①电解时,阳极的电极方程式 ;
②写出生成H2O2的反应的化学方程式: .
(4)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能降解有机污染物p-CP.控制p-CP的初始浓度相同,在不同实验条件下进行如下实验,测得p-CP的浓度随时间变化关系如图2所示.
①请根据实验I的曲线,计算降解反应
在50~150s内的反应速率ν(p-CP)= mol?L-1?s-1.
②实验Ⅰ、Ⅱ表明,温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请分析原因: .
③实验Ⅲ得出的结论是:pH=10时, .
查看习题详情和答案>>
(1)火箭推进器中分别装有联氨(N2H4)和过氧化氢,它们发生反应的热化学方程式为:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-642.2kJ?mol-1
又知:2H2O2(l)=2H2O(l)+O2(g)△H=-196.4kJ?mol-1
H2O(l)=H2O(g)△H=44kJ?mol-1
请写出N2H4(l)与O2(g)反应生成N2(g)和H2O(l) 的热化学方程式:
(2)H2O2是一种二元弱酸,其第一步电离的电离方程式为
(3)过二硫酸铵法是目前最流行的制备H2O2的方法.即电解含 H2SO4的(NH4)2SO4溶液制取(NH4)2S2O8,如图1所示,再加热水解即可得H2O2和(NH4)2SO4.

①电解时,阳极的电极方程式
②写出生成H2O2的反应的化学方程式:
(4)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能降解有机污染物p-CP.控制p-CP的初始浓度相同,在不同实验条件下进行如下实验,测得p-CP的浓度随时间变化关系如图2所示.
| 实验 编号 |
T/K | pH | c/10-3mol?L-1 | |
| H2O2 | Fe2+ | |||
| Ⅰ | 298 | 3 | 6.0 | 0.30 |
| Ⅱ | 313 | 3 | 6.0 | 0.30 |
| Ⅲ | 298 | 10 | 6.0 | 0.30 |
在50~150s内的反应速率ν(p-CP)=
②实验Ⅰ、Ⅱ表明,温度升高,降解反应速率增大.但温度过高时反而导致降解反应速率减小,请分析原因:
③实验Ⅲ得出的结论是:pH=10时,
 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:氢氧化钠少量时:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
氢氧化钠过量时:NH4HSO4+2NaOH=Na2SO4+NH3↑+2H2O
(1)同学们设计的实验装置如图所示,请回答相关问题.
①装置中碱石灰的作用是
吸收氨气中的水蒸气(干燥氨气)
吸收氨气中的水蒸气(干燥氨气)
.②广口瓶内四氯化碳的作用是
防止倒吸
防止倒吸
.③指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外泄,测得的样品含氮量仍将偏低,其原因可能是
残留在反应装置中的氨气未被稀硫酸吸收
残留在反应装置中的氨气未被稀硫酸吸收
.(2)同学们改进实验装置后(改进装置图略),进行如下实验.称取不同质量的上述样品分别与40.00mL相同浓度的氢氧化钠溶液相混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
| 氢氧化钠溶液体积/mL | 40.00mL | ||
| 样品质量/g | 7.750 | 15.50 | 23.25 |
| 氨气质量/g | 1.870 | 1.870 | 1.700 |
①样品中的氮元素的质量分数是
19.87
19.87
%.②所用氢氧化钠溶液的物质的量浓度为
3.25
3.25
mol/L.③若样品质量为31.00g,则生成氨气的质量为
1.53
1.53
g.(2012?南京模拟)实验室用硫酸铵、硫酸和废铁屑制备硫酸亚铁铵晶体的方法如下:
步骤1:将废铁屑依次用热的碳酸钠溶液、蒸馏水洗涤.
步骤2:向盛有洁净铁屑的烧杯中加入稀H2SO4溶液,水浴加热,使铁屑与稀硫酸反应至基本不再冒出气泡为止.趁热过滤.
步骤3:向滤液中加入一定量的(NH4)2SO4固体.
表1 硫酸亚铁晶体、硫酸铵、硫酸亚铁铵晶体的溶解度(g/100g H2O)
(1)步骤2中控制生成的硫酸亚铁中不含硫酸铁的方法是
(2)在0~60℃范围内,从硫酸亚铁和硫酸铵的混合溶液中可获得硫酸亚铁铵晶体的原因是
(3)为了从步骤3所得溶液中获得硫酸亚铁铵晶体,操作是
(4)测定硫酸亚铁铵晶体中Fe2+含量的步骤如下:
步骤1:准确称取硫酸亚铁铵晶体样品a g(约为0.5g),并配制成100mL溶液;
步骤2:准确移取25.0mL硫酸亚铁铵溶液于250mL锥形瓶中;
步骤3:立即用浓度约为0.1mol?L-1KMnO4溶液滴定至溶液呈稳定的粉红色,即为终点;
步骤4:将实验步骤1~3重复2次.
①步骤1中配制100mL溶液需要的玻璃仪器是
②为获得样品中Fe2+的含量,还需补充的实验是
查看习题详情和答案>>
步骤1:将废铁屑依次用热的碳酸钠溶液、蒸馏水洗涤.
步骤2:向盛有洁净铁屑的烧杯中加入稀H2SO4溶液,水浴加热,使铁屑与稀硫酸反应至基本不再冒出气泡为止.趁热过滤.
步骤3:向滤液中加入一定量的(NH4)2SO4固体.
表1 硫酸亚铁晶体、硫酸铵、硫酸亚铁铵晶体的溶解度(g/100g H2O)
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
| FeSO4?7H2O | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | - |
| (NH4)2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | - | 88.0 |
| (NH4)2SO4?FeSO4?6H2O | 12.5 | 17.2 | 21.0 | 28.1 | 33.0 | 40.0 | 44.6 |
保持铁过量
保持铁过量
.(2)在0~60℃范围内,从硫酸亚铁和硫酸铵的混合溶液中可获得硫酸亚铁铵晶体的原因是
在0~60℃范围内,同一温度下硫酸亚铁铵晶体的溶解度最小
在0~60℃范围内,同一温度下硫酸亚铁铵晶体的溶解度最小
.(3)为了从步骤3所得溶液中获得硫酸亚铁铵晶体,操作是
蒸发浓缩,冷却结晶,过滤、冰水洗涤,干燥
蒸发浓缩,冷却结晶,过滤、冰水洗涤,干燥
.(4)测定硫酸亚铁铵晶体中Fe2+含量的步骤如下:
步骤1:准确称取硫酸亚铁铵晶体样品a g(约为0.5g),并配制成100mL溶液;
步骤2:准确移取25.0mL硫酸亚铁铵溶液于250mL锥形瓶中;
步骤3:立即用浓度约为0.1mol?L-1KMnO4溶液滴定至溶液呈稳定的粉红色,即为终点;
步骤4:将实验步骤1~3重复2次.
①步骤1中配制100mL溶液需要的玻璃仪器是
玻璃棒、100mL容量瓶、胶头滴管、烧杯
玻璃棒、100mL容量瓶、胶头滴管、烧杯
.②为获得样品中Fe2+的含量,还需补充的实验是
准确测定滴定中消耗的高锰酸钾溶液的体积
准确测定滴定中消耗的高锰酸钾溶液的体积
.