网址:http://m.1010jiajiao.com/timu3_id_315932[举报]
(6分)一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
(1) 0—2 min内的平均反应速率v(HI)= 。
该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K= 。
2HI(g)的平衡常数K= 。
(2)相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
(6分)一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
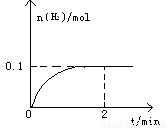
(1) 0—2 min内的平均反应速率v(HI)= 。
该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=
。
2HI(g)的平衡常数K=
。
(2) 相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
查看习题详情和答案>>
 H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
(1) 0—2 min内的平均反应速率v(HI)= 。
该温度下,H2(g)+I2(g)
 2HI(g)的平衡常数K= 。
2HI(g)的平衡常数K= 。(2)相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
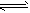 H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
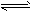 2HI(g)的平衡常数K=_________。
2HI(g)的平衡常数K=_________。(2)相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_________是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
(3)以H2为燃料可制成氢氧燃料电池。 已知2H2(g)+O2(g)==2H2O(l) △H=-572kJ/mol-1
某氢氧燃料电池释放228.8kJ电能时,生成1mol液态水,该电池的能量转化率为___________。
 一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)
一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)![]() H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
(1) 0—2 min内的平均反应速率v(HI)= 。该温度下,H2(g)+I2(g)![]() 2HI(g)的平衡常数K= 。
2HI(g)的平衡常数K= 。
(2) 相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
(3)以H2为燃料可制成氢氧燃料电池。
已知 2H2(g)+O2(g)===2H2O(l) △H=-572KJ.mol-1
某氢氧燃料电池释放228.8KJ电能时,生成1mol液态水,该电池的能量转化率为 。
查看习题详情和答案>>