题目内容
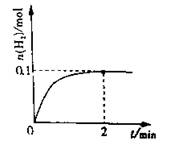
(6分)一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
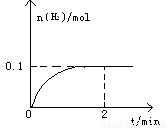
(1) 0—2 min内的平均反应速率v(HI)= 。
该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=
。
2HI(g)的平衡常数K=
。
(2) 相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
【答案】
0.1 mol/(L·min) 80 b (每空2分)
【解析】 (1)根据图像可知,0—2 min内,氢气的的物质的量增加了0.1mol,则必然消耗HI是0.2mol,使用平均反应速率v(HI)=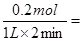 0.1 mol/(L·min) ;平衡时氢气和碘的浓度都是0.1mol/L,而碘化氢的是0.8mol/L,使用该温度下平衡常数K=
0.1 mol/(L·min) ;平衡时氢气和碘的浓度都是0.1mol/L,而碘化氢的是0.8mol/L,使用该温度下平衡常数K=
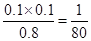 ,所以逆反应的平衡常数是80。
,所以逆反应的平衡常数是80。
(2)平衡常数只与温度有关系,选项a不正确。由于反应前后体积不变,所以该反应是等效的,因此选项b正确,d不正确;浓度增加,反应时间增大,达到平衡的时间减少,选项c不正确,答案选b。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定温度下,向1L密闭容器中通入0.2mol NO和0.1molBr2,保持一定条件发生反应:
2NO(g)+Br2(g)=2NOBr(g)中.Br2的物质的量n(Br2)随时间变化的实验数据如下表:
根据表中数据,下列说法正确的是( )
2NO(g)+Br2(g)=2NOBr(g)中.Br2的物质的量n(Br2)随时间变化的实验数据如下表:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| n(Br2)/mol | 0.080 | 0.075 | 0.072 | 0.070 | 0.070 | 0.070 |
| A、20 min后浓度不再变化,是因为反应已停止 |
| B、10 min内Br2的平均反应速率是0.0025 mol/(L?min) |
| C、25 min~30 min过程中,NO的物质的量浓度逐渐降低 |
| D、20 min时,容器中NO和Br2的物质的量浓度相等 |
 (2010?山东)硫一碘循环分解水制氢主要涉及下列反应:
(2010?山东)硫一碘循环分解水制氢主要涉及下列反应: H2+I2
H2+I2 2HI(g)的平衡常数K=
2HI(g)的平衡常数K= (2011?南开区一模)能源开发、环境保护、资源利用等是当今社会的热门话题.请根据所学化学知识回答下列问题:
(2011?南开区一模)能源开发、环境保护、资源利用等是当今社会的热门话题.请根据所学化学知识回答下列问题: 硫一碘循环分解水制氢主要涉及下列反应:
硫一碘循环分解水制氢主要涉及下列反应: