摘要:计算题 室温时20 mL某气态烃与过量的氧气混合.完全燃烧后的产物通过浓硫酸.再恢复到至室温.气体体积减少了50 mL .剩余气体再通过氢氧化钠溶液.体积又减少了40 mL .求气态烃的分子式. 附加题:(附加分5分计入总分.但总分不超过100分) . A是芳香烃的含氧衍生物.为了测定其分子组成.进行如下实验: ①在一定温度和压强下将A气化.其气体的质量是同温.同压下等体积氦气质量的38倍,②称取7.6gA.在11.2L氧气中完全燃烧.其产物只有CO2和水蒸气.将反应后的混合气通过浓硫酸后体积为10.64L.浓H2SO4质量增加3.6g.再将余下的气体通过盛有足量Na2O2的干燥管后.气体体积减少至6.16L(气体体积均在标准状况下测定).试回答: ⑴A的化学式为 . ⑵A物质中只有一条支链.遇FeCl3溶液无显色反应.1molA只能与1molNaHCO3反应,1molA与足量Na反应生成1molH2.则A的结构简式为 . 杭高2010学年第一学期期中考试高二化学答卷页 卷I 选择题 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 卷II 简答题 24.(1)写出以下物质的结构简式 ① 2.3-二甲基-4-乙基已烷 ② TNT (2)写出下列反应的方程式 ①CH3CH2CHO + Cu(OH)2 ② + H2 ③ + O2
网址:http://m.1010jiajiao.com/timu3_id_315641[举报]
室温时20 mL某气态烃与过量的氧气混合,完全燃烧后的产物通过浓硫酸,再恢复到至室温,气体体积减少了50 mL ,剩余气体再通过氢氧化钠溶液,体积又减少了40 mL 。求气态烃的分子式 查看习题详情和答案>>
查看习题详情和答案>>
已知室温时,某一元酸HA溶液用pH计测定其pH=4.0.另取20.00mL此一元酸HA溶液,用0.2000mol/L的NaOH溶液滴定,用去NaOH溶液10.00ml.试计算此酸在室温时:
(1)电离度(α),
(2)电离常数(Ka).
查看习题详情和答案>>
(1)电离度(α),
(2)电离常数(Ka).
 Ⅰ.室温时1L 0.01mol?L-1的硫酸氢钠溶液的pH为
Ⅰ.室温时1L 0.01mol?L-1的硫酸氢钠溶液的pH为2
2
,在其中滴入等体积的0.01mol?L-1的Ba(OH)2溶液后,加水稀释到10L,所发生反应的离子方程式为Ba2++OH-+H++SO42-═BaSO4↓+H2O
Ba2++OH-+H++SO42-═BaSO4↓+H2O
,pH为11
11
.Ⅱ.某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)
①
①
,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)偏大
偏大
.(2)判断滴定终点的现象是:
无色变为粉红,半分钟内不变色
无色变为粉红,半分钟内不变色
.(3)如下图是某次滴定时的滴定管中的液面,其读数为
22.60
22.60
mL.(4)根据下列数据:请计算待测盐酸溶液的浓度:
0.2000
0.2000
mol/L.| 滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
氯化铁是常见的水处理剂,无水FeCl3的熔点为555K、沸点为588K.工业上制备无水FeCl3的一种工艺如下:
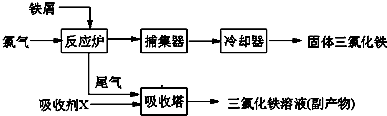
(1)试写出吸收塔中反应的离子方程式:
(2)已知六水合氯化铁在水中的溶解度如下:
从FeCl3溶液中获得FeCl3?6H2O的方法是:
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的分子式为:
(4)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)=
(5)FeCl3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c mol/L Na2S2O3溶液滴定用去V mL.(已知:I2+2S2O32-=2I-+S4O62-)
①滴定终点的现象是:
②样品中氯化铁的质量分数为:
%
%.
③某同学根据上述方案,使用上述(2)中获得的FeCl3?6H2O样品代替无水氯化铁样品进行测定.通过计算发现产品中的质量分数大于100%,其原因可能是
查看习题详情和答案>>

(1)试写出吸收塔中反应的离子方程式:
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(2)已知六水合氯化铁在水中的溶解度如下:
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH20) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
加入少量盐酸加热浓缩,再冷却结晶
加入少量盐酸加热浓缩,再冷却结晶
.(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的分子式为:
Fe2Cl6
Fe2Cl6
.(4)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)=
1.1×10-6
1.1×10-6
mol/L(已知:Ksp[Fe(OH)3]=1.1×10-36).(5)FeCl3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用c mol/L Na2S2O3溶液滴定用去V mL.(已知:I2+2S2O32-=2I-+S4O62-)
①滴定终点的现象是:
滴入最后一滴,溶液颜色由蓝色变为无色,半分钟内不再变色
滴入最后一滴,溶液颜色由蓝色变为无色,半分钟内不再变色
.②样品中氯化铁的质量分数为:
| 162.5cV |
| m |
| 162.5cV |
| m |
③某同学根据上述方案,使用上述(2)中获得的FeCl3?6H2O样品代替无水氯化铁样品进行测定.通过计算发现产品中的质量分数大于100%,其原因可能是
FeCl3?6H2O烘干时失去了部分结晶水
FeCl3?6H2O烘干时失去了部分结晶水
.(8分)20℃时,醋酸的电离平衡常数为1.6×10-5。
(1)试计算20℃时0.01mol•L-1的醋酸溶液中氢离子浓度。
(2)室温时,向0.2mol•L-1的醋酸溶液中加入等体积的0.1mol•L-1的NaOH(aq),充分反应后所得溶液的PH=4,则:
①所得溶液中各离子(包括CH3COOH分子)浓度大小关系是:______________________,
②所得溶液中的物料守恒式为:________+________=__________=_________mol•L-1。
③c(CH3COOH)=_____________mol•L-1(写出算式,不做近似计算)
查看习题详情和答案>>