摘要:10.在400 ℃.催化剂存在下.向容积固定为l0 L的密闭容器中充入0.2 mol SO2和0.19 mol O2.3 min时达到平衡.测得SO2的浓度为0.002 mol/L.下列叙述错误的是 A.反应开始至3 min内.(O2)=0.006 mol/ B.容器内压强不再变化时表明反应已达平衡状态 C.平衡混合物中SO3的体积分数为60% D.相同条件下.如在原容器中充入的是0.2 mol SO3和0.09 mol O2.达到平衡后c(SO2)=0.002 mol/L
网址:http://m.1010jiajiao.com/timu3_id_299289[举报]
(2010?上海)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)?2SO3(g)+190kJ
1)该反应所用的催化剂是
2)该热化学反应方程式的意义是
3)对于反应2SO2+O2?2SO3(g),化学平衡状态的标志为
a.v正(O2)=2v正(SO3)
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=
查看习题详情和答案>>
2SO2(g)+O2(g)?2SO3(g)+190kJ
1)该反应所用的催化剂是
五氧化二钒
五氧化二钒
(填写化合物名称),该反应450℃时的平衡常数大于
大于
500℃时的平衡常数(填“大于”、“小于”或“等于”).2)该热化学反应方程式的意义是
在450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ
在450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ
.3)对于反应2SO2+O2?2SO3(g),化学平衡状态的标志为
bd
bd
a.v正(O2)=2v正(SO3)
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=
0.036
0.036
mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,则平衡向正反应方向
向正反应方向
移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,0.36
0.36
mol<n(SO3)<0.40
0.40
mol. 2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法中错误的是( )
2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法中错误的是( ) 在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.下列说法不正确的是( )
在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.下列说法不正确的是( )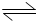 2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )