题目内容
工业制硫酸中一步重要的反应是:SO2在400~500℃的条件下进行催化氧化:2SO2+O2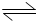 2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
 2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )分析:该反应是前后气体体积减小的放热反应,根据外界条件对化学平衡的影响因素分析.
解答:解:该反应是前后气体体积减小的放热反应.
A、使用催化剂加快了反应速率,缩短反应时间,提高反应效率,故A正确;
B、该反应是可逆反应,所以该反应存在反应限度,反应物不可能100%的转化,反应达平衡时容器中存在SO2、O2、SO3三种物质,故B正确;
C、该反应是一个放热反应,放出的能量可以使反应进行,故C错误;
D、达到平衡时,SO2的浓度与SO3的浓度可能相等,也可能不相等,要看反应物的初始浓度及转化率,故D正确.
故选C.
A、使用催化剂加快了反应速率,缩短反应时间,提高反应效率,故A正确;
B、该反应是可逆反应,所以该反应存在反应限度,反应物不可能100%的转化,反应达平衡时容器中存在SO2、O2、SO3三种物质,故B正确;
C、该反应是一个放热反应,放出的能量可以使反应进行,故C错误;
D、达到平衡时,SO2的浓度与SO3的浓度可能相等,也可能不相等,要看反应物的初始浓度及转化率,故D正确.
故选C.
点评:本题考查了影响化学平衡移动的因素,难度不大,注意催化剂只影响化学反应速率不影响化学平衡.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
工业制硫酸的一步重要反应是SO2在400~500℃的催化氧化:2SO2+O2 2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述说法中错误的是
2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述说法中错误的是
| A.在上述条件下,SO2不可能100%转化为SO3 |
| B.达到平衡时,SO2、SO3的物质的量浓度相等 |
| C.使用催化剂可以加快反应速率,提高生产效率 |
| D.适当提高O2的浓度,可以提高SO2的转化率 |
 2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述说法中错误的是
2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述说法中错误的是
 2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )
2SO3,其正反应为放热反应.如果该反应是在密闭容器中进行的,下述有关说法中错误的是( )