题目内容
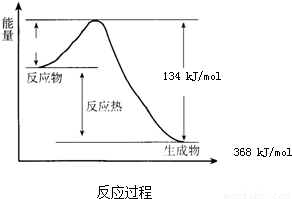
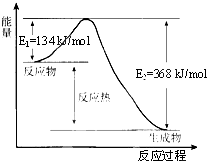 在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.下列说法不正确的是( )
在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.下列说法不正确的是( )分析:A、由图象可知,该反应是一个能量降低的反应,即放热反应;
B、反应的焓变=拆化学键吸收能量-形成化学键放出能量;
C、加入催化剂,使该反应的活化能降低,同等程度的改变正逆反应的活化能;
D、热化学方程式反写时,反应热数值不变,符号相反.
B、反应的焓变=拆化学键吸收能量-形成化学键放出能量;
C、加入催化剂,使该反应的活化能降低,同等程度的改变正逆反应的活化能;
D、热化学方程式反写时,反应热数值不变,符号相反.
解答:解:A、由图象可知,该反应是一个能量降低的反应,即放热反应,故A正确;
B、反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234kJ/mol,故B正确;
C、加入催化剂,使该反应的活化能降低,同等程度的改变正逆反应的活化能,所以反应热的值不变,故C错误;
D、热化学方程式反写时,反应热数值不变,符号相反,所以NO(g)+CO2(g)
NO2(g)+CO(g)△H=+234 kJ/mol,故D正确.
故选C.
B、反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234kJ/mol,故B正确;
C、加入催化剂,使该反应的活化能降低,同等程度的改变正逆反应的活化能,所以反应热的值不变,故C错误;
D、热化学方程式反写时,反应热数值不变,符号相反,所以NO(g)+CO2(g)
| ||
| 101kPa |
故选C.
点评:本题考查了反应热、活化能、催化剂对活化能的影响等,难度中等,注意催化剂对反应热无影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示.
在400℃、101kPa时,NO2(g)+CO(g)?NO(g)+CO2(g)反应过程的能量变化如图所示.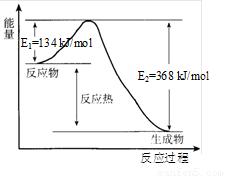
 NO2(g)+CO(g)△H
=+234 kJ/mol
NO2(g)+CO(g)△H
=+234 kJ/mol