摘要:23. (1)按系统命名法. 的名称是 ▲ , (2)写出CH3CO18OC2H5与稀硫酸共热反应的化学方程式(要标出18O的位置): ▲ .
网址:http://m.1010jiajiao.com/timu3_id_298734[举报]
 Ⅰ.铜与稀硝酸反应的离子方程式为
Ⅰ.铜与稀硝酸反应的离子方程式为在做铜与稀硝酸反应的实验时,常观察到试管内生成的气体先为浅红棕色,其原因是
为了能直接观察到生成的气体的颜色,可在往稀硝酸中加入铜的同时,加入少量碳酸盐,那么加入少量碳酸盐的作用是
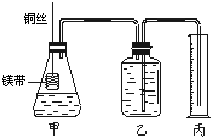
Ⅱ.某研究性学习小组欲证明:在同温同压下,相同浓度、相同体积的酸性不同的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如右图所示.该实验的主要操作步骤如下:
①配制浓度均为1mol?L-1盐酸和醋酸溶液;
②量取15.00mL 1mol?L-1盐酸和醋酸溶液分别加入两个锥形瓶中;
③分别称取除去表面氧化膜的镁带a g,并系于铜丝末端;
④在广口瓶中装足量的水,按图连接好装置,检查装置的气密性;
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触),至反应完全,记录相关数据;
⑥反应结束后待温度恢复到室温,调整乙和丙中液面使二者处于同一平面,读出量筒中水的体积为V mL.
请你参与实验并回答下列问题:
(1)量取15.00mL 1mol?L-1盐酸和醋酸溶液所用的仪器是
A.带刻度的烧杯 B.量筒 C.酸式滴定管 D.碱式滴定管
(2)步骤③中a的数值至少是
(3)本实验装置丙中量筒的规格是
A.10mL B.100mL C.200mL D.500mL
(4)若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积的计算式为:Vm=
(5)试简述速率不等的原因是
(6)试写出镁与醋酸溶液反应的离子方程式:
(2011?开封一模)“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请你回答以下问题:
(1)无机非金属材料.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.这种材料可以按下列方法制备:
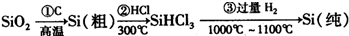
①写出步骤①的化学方程式
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3的主要化学操作的名称是
③请写出二氧化硅与氢氟酸反应的化学方程式
(2)磁性材料.这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护.最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式
(3)激光材料.我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
(4)纳米材料.胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是
(5)高分子材料.可以分成无机高分子材料和有机高分子材料.一种新型高效净水剂
[AlFe(OH)nCl6-n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为
一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH-CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式
 .
.
查看习题详情和答案>>
(1)无机非金属材料.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”.这种材料可以按下列方法制备:
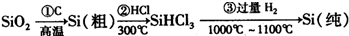
①写出步骤①的化学方程式
SiO2+2C
Si+2CO↑
| ||
SiO2+2C
Si+2CO↑
.
| ||
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3的主要化学操作的名称是
蒸馏(或分馏)
蒸馏(或分馏)
.③请写出二氧化硅与氢氟酸反应的化学方程式
SiO2+4HF=SiF4↑+2H2O
SiO2+4HF=SiF4↑+2H2O
.(2)磁性材料.这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护.最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式
Fe→Fe2++2e-
Fe→Fe2++2e-
.(3)激光材料.我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
Al2O3+6H+═2Al3++3H2O
Al2O3+6H+═2Al3++3H2O
,Al2O3+2OH-+3H2O=2[Al(OH)4]-
Al2O3+2OH-+3H2O=2[Al(OH)4]-
.(4)纳米材料.胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是
1nm~100nm
1nm~100nm
,三氯化铁溶液可以加速伤口止血,请简述原因氯化铁是电解质,使血液胶体聚沉
氯化铁是电解质,使血液胶体聚沉
.(5)高分子材料.可以分成无机高分子材料和有机高分子材料.一种新型高效净水剂
[AlFe(OH)nCl6-n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为
+3
+3
.一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH-CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式


在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.下图所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.

(1)实验室若用NH4Cl和熟石灰作试剂来制取、收集干燥的NH3,则需选用上述仪器装置中的
(2)若在A的分液漏斗内改加浓氨水,圆底烧瓶内加NaOH固体,也能制取氨气.请解释装置A中能产生氨气的原因
(3)向浓CaCl2溶液中通入NH3和CO2气制纳米级碳酸钙时,应先通入的气体是

写出制纳米级碳酸钙的化学方程式
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
查看习题详情和答案>>

(1)实验室若用NH4Cl和熟石灰作试剂来制取、收集干燥的NH3,则需选用上述仪器装置中的
BDE
BDE
(填装置序号).若要制取、收集干燥的CO2,请选择装置并按气流方向连接各仪器接口acdh
acdh
.(2)若在A的分液漏斗内改加浓氨水,圆底烧瓶内加NaOH固体,也能制取氨气.请解释装置A中能产生氨气的原因
氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠吸水,促使氨放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出
氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠吸水,促使氨放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出
.(3)向浓CaCl2溶液中通入NH3和CO2气制纳米级碳酸钙时,应先通入的气体是
NH3
NH3
,若实验过程中有氨气逸出,应选用下列b
b
装置回收(填代号).
写出制纳米级碳酸钙的化学方程式
CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
.(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
.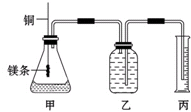 某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:
某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积.设计的简易实验装置如图.该实验的主要操作步骤如下:Ⅰ.(1)配制浓度均为0.50mol?L-1 H2SO4和H2C2O4溶液;
(2)用
(3)分别称取除去表面氧化膜的镁条并系于铜丝末端;
(4)检查装置的气密性,在广口瓶中装满水,按图连接好装置;
(5)将铜丝向下移动,使足量镁条浸入酸中(铜丝不能与酸接触),至反应完全,记录
(6)反应结束后,读取量筒中水的体积为y mL.
Ⅱ.请将上述步骤补充完整并回答下列问题:
(1)用密度为1.84g?cm-3 98%的浓硫酸配制250mL 0.50mol?L-1的H2SO4溶液,所需要的主要仪器有
(2)以下是读取量筒内水的体积时必须包括的几个步骤:①使乙、丙中液面相平;②将装置冷却至室温;③读取量筒内水的体积.这三步操作的正确顺序是
(3)读取量筒内水的体积时,若丙中液面高于乙中液面,使乙、丙中液面相平的操作是
(4)简述速率不等的原因是
 如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:
如图1和2是某校实验探究小组制备NH3 并进行性质实验时的改进装置.按图1把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化锅覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL浓氨水);烧杯内盛滴有酚酞试液的水.把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.将上述装置中收满NH3的圆底烧瓶取下,改装成图2所示的装置,胶头滴管内事先吸入2mLH2O,此时小气球系在玻璃管上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某个性质.按要求回答下列问题:(1)教材中是用与制O2相同的制备装置来加热制取NH3的,该反应的化学方程式为:
2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2
| ||
2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2
.
| ||
(2)下面是部分同学对于能用图1制取NH3的原因分析,有道理的是
①②③④
①②③④
.①在NH3?H2O中有平衡 NH3+H2O=NH3?H2O=NH4++OH-,NaOH使平衡向左移动; ②在NH3?H2O中有平衡阳NH3+H2O=NH3?H2O=NH4++OH-,NH4Cl 使平衡向左移动; ③NaOH 溶于水时放热,使体系的温度升高,NH3的溶解度减小;④NH4Cl与NaOH在此情况下可反应生成NH3,即NH4++OH-
| ||
(3)判断图1中烧瓶己收满NH3的现象
烧杯内的溶液变红
烧杯内的溶液变红
.(4)图2中胶头漓管中的水挤入烧瓶后,观察到的现象是
气球逐渐变大
气球逐渐变大
它说明了NH3极易溶于水
极易溶于水
.