网址:http://m.1010jiajiao.com/timu3_id_286895[举报]
A、C两种元素的原子的最后一个电子都填充在s亚层中,1 mol的A单质同水反应生成1 g H2,同时转化为具有Ne原子电子层结构的离子。B的核电荷数比A少5个,B与C可形成正四面体的共价化合物D,原子半径A、B、C依次递减,试判断:
(1)A、B、C各为何种元素?
(2)哪个元素的原子最外层的电子能量最高?写出能量最高的电子所处的电子亚层符号。
(3)写出D的电子式和结构式。
(4)写出A的氧化物的电子式。
查看习题详情和答案>>
(1)写出F的电子式


(2)气体H有毒,可用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:
(3)加热E的水溶液后并灼烧,最终得到的固体为
| ||
| ||
(4)室温下,向F的水溶液中加入等体积等浓度的盐酸反应后所得溶液的PH>7,则此溶液中离子浓度由小到大的顺序为:
(5)将气体H放在空气中充分燃烧可得到气体氧化物BO2,BO2可与氧气继续反应:2BO2+O2
 2BO3,在一个固定容积为2L的密闭容器中充入0.20mol的BO2和0.10mol的O2,半分钟后达到平衡,测得容器中含BO3为0.18mol,则v(o2 )=
2BO3,在一个固定容积为2L的密闭容器中充入0.20mol的BO2和0.10mol的O2,半分钟后达到平衡,测得容器中含BO3为0.18mol,则v(o2 )=(1)B与D形成化合物BD2的结构式为
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式
| ||
| ||
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为
 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH-(4)C2A4─空气燃料电池是一种碱性燃料电池.电解质溶液是20%~30%的KOH溶液.则燃料电池放电时:正极的电极反应式是
(5)已知:2CD2(g)
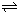 C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.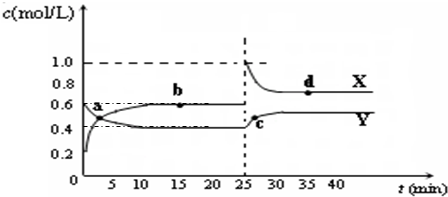
①a、b、c、d四个点中,化学反应处于平衡状态的是
②25min时,增加了
③a、b、c、d四个点所表示的反应体系中,气体颜色由深到浅的顺序是
 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应.(1)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,反应后溶液呈浅绿色.则A在元素周期表中的位置是
(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,③和④两个反应中都有红棕色气体生成,反应①的化学方程式是
| ||
| ||
| ||
| ||
(3)若A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是
 Si+2CO↑
Si+2CO↑ Si+2CO↑
Si+2CO↑A、B、C、D是常见不同主族的短周期元素,它们的原子序数逐渐增大,其中只有一种是金属元素,C元素原子最外层电子数是D元素原子最外层电子数的一半,B元素原子的最外层电子数比D的最外层电子数少两个。E、F也是短周期元素,E与D同主族,F与A同主族。
(1)写出F2E2的电子式 。其中化学键类型为__________________。
(2)A 、 E 、 F 三种元素可形成一种离子化合物 R ,用惰性电极电解 R 的稀溶液的化学反应方程式为_________________________________;电解一段时间后,溶液 pH_____(填“增大”、“减小”或“不变”)。
(3)六种元素中的三种组成的易溶于水的酸性物质中,能促进水电离的物质M是 (写化学式,写一个即可,下同),能抑制水电离的物质N是 。25℃时,pH=a的M溶液中水电离出的H+浓度与pH=a的N溶液中水电离出的H+浓度之比为 。
(4)甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同。回答问题:
①向乙溶液中缓慢滴加过量的丙溶液过程中发生反应的离子方程式 ;
②向甲溶液中缓慢滴加过量的丙溶液,所观察到的实验现象为 。
查看习题详情和答案>>