题目内容
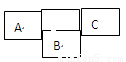
A、C两种元素的原子的最后一个电子都填充在s亚层中,1 mol的A单质同水反应生成1 g H2,同时转化为具有Ne原子电子层结构的离子。B的核电荷数比A少5个,B与C可形成正四面体的共价化合物D,原子半径A、B、C依次递减,试判断:
(1)A、B、C各为何种元素?
(2)哪个元素的原子最外层的电子能量最高?写出能量最高的电子所处的电子亚层符号。
(3)写出D的电子式和结构式。
(4)写出A的氧化物的电子式。
(1)A:Na B:C C:H (2)Na 3S1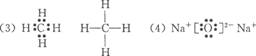
(4) ![]()

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
A、B、C为短周期元素,在周期表中如表所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法不正确的是( )
| A | D | C |
| B |
| A、A的氧化物有多种形式 |
| B、B的最高价氧化物对应的水化物是一种强酸 |
| C、C的氢化物水溶液通常用玻璃试剂瓶盛放 |
| D、D元素形成的单质不止一种 |
 如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.
如图示是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等.