网址:http://m.1010jiajiao.com/timu3_id_281042[举报]

(1)则
② 。
(2)
(3)
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析原因: ⑤ 。
查看习题详情和答案>>已知水在25 ℃和95 ℃时,其电离平衡曲线如右图所示:
⑴则25 ℃时水的电离平衡曲线应为 ___ (填“A”或“B”),请说明理由 ________________ 。
⑵95 ℃时PH=2的NaOH溶液中由水电离的c(H+) ______。
⑶25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 _________ 。
⑷25 ℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 _____ 。
⑸曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析原因: 。
⑹95 ℃时,某氨水与氯化铵的混合溶液的PH=7,则c(NH4+)______c(Cl-)(填“>”、“<”、或“=”)
已知水在25℃和95℃时,其电离平衡曲线如右图所示: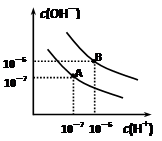
⑴则25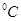 时水的电离平衡曲线应为 (填“A”或“B”)。
时水的电离平衡曲线应为 (填“A”或“B”)。
⑵25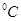 时,将
时,将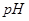 =8的NaOH溶液与
=8的NaOH溶液与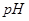 =5的
=5的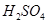 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的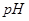 =7,则NaOH溶液与
=7,则NaOH溶液与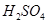 溶液的体积比为 。
溶液的体积比为 。
⑶95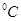 时,0.1 mol/L的NaOH溶液的pH值是 。
时,0.1 mol/L的NaOH溶液的pH值是 。
⑷95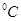 时,若100体积
时,若100体积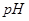 1=
1=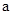 的某强酸溶液与1体积
的某强酸溶液与1体积 2=b的某强碱溶液混合后溶液呈中性,则混合前,
2=b的某强碱溶液混合后溶液呈中性,则混合前,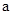 与b之间应满足的关系是
与b之间应满足的关系是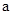 = (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
= (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
已知水在25℃和95℃时,其电离平衡曲线如右图所示:
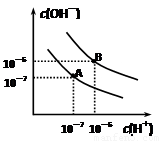
⑴则25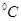 时水的电离平衡曲线应为 (填“A”或“B”)。
时水的电离平衡曲线应为 (填“A”或“B”)。
⑵25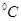 时,将
时,将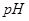 =8的NaOH溶液与
=8的NaOH溶液与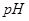 =5的
=5的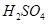 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的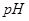 =7,则NaOH溶液与
=7,则NaOH溶液与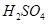 溶液的体积比为 。
溶液的体积比为 。
⑶95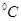 时,0.1 mol/L的NaOH溶液的pH值是 。
时,0.1 mol/L的NaOH溶液的pH值是 。
⑷95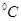 时,若100体积
时,若100体积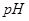 1=
1=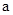 的某强酸溶液与1体积
的某强酸溶液与1体积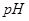 2=b的某强碱溶液混合后溶液呈中性,则混合前,
2=b的某强碱溶液混合后溶液呈中性,则混合前,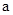 与b之间应满足的关系是
与b之间应满足的关系是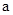 = (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
= (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
查看习题详情和答案>>
已知水在25 ℃和95 ℃时,其电离平衡曲线如右图所示:

⑴则25 ℃时水的电离平衡曲线应为 ___ (填“A”或“B”),请说明理由 ________________ 。
⑵95 ℃时PH=2的NaOH溶液中由水电离的c(H+) ______。
⑶25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 _________ 。
⑷25 ℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 _____ 。
⑸曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。请分析原因: 。
⑹95 ℃时,某氨水与氯化铵的混合溶液的PH=7,则c(NH4+)______c(Cl-)(填“>”、“<”、或“=”)
查看习题详情和答案>>