网址:http://m.1010jiajiao.com/timu3_id_274353[举报]

(1)容器中气体出现红棕色的原因(用化学方程式表示)是__________________________。
(2)前2 s内,乙容器中以N2O4的浓度变化表示的反应速率为____________。
(3)达到平衡时,甲容器中反应所需的时间__________60 s(填“大于”“小于”或“等于”,以下同);两容器中都达到平衡时,N2O4的浓度甲______乙;反应过程中吸收的能量甲______乙。?
(4)两容器都达到平衡后,若要使甲、乙中N2O4浓度相等,不能采取的措施是_________。
A.保持温度不变,适当压缩甲容器体积?
B.保持容器体积不变,使甲容器升温?
C.保持容器体积和温度不变,向甲容器中加入适量N2O4
查看习题详情和答案>>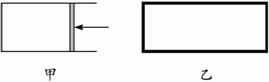
(1)容器中气体出现红棕色的原因(用化学方程表示)是___________________。?
(2)前2 s内乙容器中以N2O4的浓度变化表示的反应速率为_____________________。
(3)达到平衡时,甲容器中反应所需要的时间______________60 s(填“大于”“小于”或“等于”);反应过程中吸收的能量甲_____________(填“大于”“小于”或“等于”)乙。
(4)若要使甲、乙中N2O4浓度相等,不能采取的措施是_____________(填选项的标号)。
A.保持温度不变,适当压缩甲容器体积
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量N2O4
查看习题详情和答案>>一定温度下,分别往容积均为5 L的甲(恒压密闭容器)、乙(恒容密闭容器)中各加入0.5 mol无色的N2O4气体,立即出现红棕色。当反应进行到2 s时,测得乙容器中N2O4的浓度为0.09 mol·L-1。经过60 s乙容器中的反应达到平衡(反应过程中两个容器的温度均保持恒定)。

(1)容器中气体出现红棕色的原因是(用化学方程式表示)
________________________________________________________________________。
(2)前2 s内,乙容器中以N2O4的浓度变化表示的平均反应速率为____________________。
(3)达到平衡时,甲容器中反应所需的时间______60 s(填“大于”、“小于”或“等于”,下同);两容器中都达到平衡时,N2O4的浓度:甲__________乙,反应过程中吸收的能量:甲__________乙。
(4)两容器都达到平衡后,若要使甲、乙中N2O4浓度相等,不能采取的措施是__________。
A.保持温度不变,适当压缩甲容器
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量N2O4
D.保持容器体积不变,使甲容器降温
查看习题详情和答案>>
一定温度下,分别往容积均为5 L的甲(恒压密闭容器)、乙(恒容密闭容器)中各加入0.5 mol无色的N2O4气体,立即出现红棕色.当反应进行到2 s时,测得乙容器中N2O4的浓度为0.09 mol/L.经过60 s乙容器中的反应达到平衡(反应过程中两个容器的温度均保持恒定)

(1)容器中气体出现红棕色的原因(用化学方程式表示)是________;
(2)前2 s内,乙容器中以N2O4的浓度变化表示的反应速率为________;
(3)达到平衡时,甲容器中反应所需的时间________60 s(填“大于”“小于”或“等于”,以下同);两容器中都达到平衡时,N2O4的浓度甲________乙;反应过程中吸收的能量甲________乙.
(4)两容器都达到平衡后,若要使甲、乙中N2O4浓度相等,不能采取的措施是________
A.保持温度不变,适当压缩甲容器体积
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量N2O4