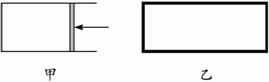题目内容
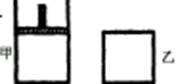
一定温度下,分别往容积均为5 L的甲(恒压密闭容器)、乙(恒容密闭容器)中各加入0.5 mol无色的N2O4气体,立即出现红棕色。当反应进行到2 s时,测得乙容器中N2O4的浓度为0.09 mol·L-1。经过60 s乙容器中的反应达到平衡(反应过程中两个容器的温度均保持恒定)。

(1)容器中气体出现红棕色的原因是(用化学方程式表示)
________________________________________________________________________。
(2)前2 s内,乙容器中以N2O4的浓度变化表示的平均反应速率为____________________。
(3)达到平衡时,甲容器中反应所需的时间______60 s(填“大于”、“小于”或“等于”,下同);两容器中都达到平衡时,N2O4的浓度:甲__________乙,反应过程中吸收的能量:甲__________乙。
(4)两容器都达到平衡后,若要使甲、乙中N2O4浓度相等,不能采取的措施是__________。
A.保持温度不变,适当压缩甲容器
B.保持容器体积不变,使甲容器升温
C.保持容器体积和温度不变,向甲容器中加入适量N2O4
D.保持容器体积不变,使甲容器降温
(1)N2O4 2NO2 (2)0.005
mol·L-1·s-1 (3)大于 小于 大于 (4)B
2NO2 (2)0.005
mol·L-1·s-1 (3)大于 小于 大于 (4)B
【解析】
试题分析:(1)因为N2O4 2NO2,故无色气体会出现红棕色。
2NO2,故无色气体会出现红棕色。
(2)前2 s内v(N2O4)=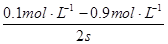 =0.005 mol·L-1·s-1。
=0.005 mol·L-1·s-1。
(3)由于反应N2O4 2NO2是一个气体体积增大的反应,随着反应的进行,V甲>V乙,p乙>
p甲,压强大,化学反应速率快,故乙容器先达平衡,所以甲容器中反应达平衡所需时间大于60 s。由于甲中压强不变,故达到平衡时,甲中四氧化二氮的浓度小于乙中四氧化二氮的浓度。由于反应N2O4
2NO2是一个气体体积增大的反应,随着反应的进行,V甲>V乙,p乙>
p甲,压强大,化学反应速率快,故乙容器先达平衡,所以甲容器中反应达平衡所需时间大于60 s。由于甲中压强不变,故达到平衡时,甲中四氧化二氮的浓度小于乙中四氧化二氮的浓度。由于反应N2O4 2NO2是一个吸热反应,而增大压强有利于反应向逆反应方向进行,故反应过程中吸收的热量甲大于乙。
2NO2是一个吸热反应,而增大压强有利于反应向逆反应方向进行,故反应过程中吸收的热量甲大于乙。
(4)因甲中四氧化二氮的浓度小于乙中四氧化二氮的浓度,若使两者浓度相等,则应使甲中N2O4浓度增大或使乙中N2O4的浓度减小,其中A、C、D都能使N2O4(甲中)的浓度增大。
考点:考查可逆反应、反应速率的计算和应用、能量变化、浓度比较以及外界条件对平衡状态的影响
点评:该题综合性强,贴近高考,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和创新思维能力,提高学生的应试能力。

 如图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色.当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol?L-1.经过 60s,乙容器中的反应达到平衡.(反应过程中两个容器的温度均保持恒定)
如图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色.当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol?L-1.经过 60s,乙容器中的反应达到平衡.(反应过程中两个容器的温度均保持恒定)