下列物质的工业制备原理的方程式书写正确的是
A.乙醇:C6H12O6 2CH3CH2OH+2CO2↑ 2CH3CH2OH+2CO2↑ |
B.乙烯:CH3CH2OH CH2=CH2↑+ H2O CH2=CH2↑+ H2O |
C.盐酸:NaCl+H2SO4 NaHSO4+HCl↑ NaHSO4+HCl↑ |
| D.纯碱:2NaCl+2NH3+CO2+H2O → Na2CO3↓+ 2NH4Cl |
CaCO3是一种化工原料,可以通过反应生成一系列物质,如下图所示。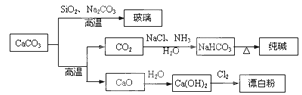
下列说法正确的是
| A.Cl2和SO2均可以漂白有色物质,且漂白的原理相同 |
B.由SiO2+Na2CO3 Na2SiO3+CO2↑可知,H2CO3的酸性强于H2SiO3 Na2SiO3+CO2↑可知,H2CO3的酸性强于H2SiO3 |
| C.工业上,可先向饱和食盐水中通入NH3后,再通入CO2制NaHCO3 |
| D.制取玻璃、纯碱和漂白粉所涉及的反应都是非氧化还原反应 |
在H2SO4、HNO3、NH3的工业生产中,具有的共同点是
| A.使用H2作原料 | B.使用催化剂 |
| C.使用吸收塔设备 | D.使用尾气吸收装置 |
对于可逆反应N2(g)+3H2(g) 2NH3(g)(正反应为放热反应),下列说法中正确的是( )。
2NH3(g)(正反应为放热反应),下列说法中正确的是( )。
| A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,H2的浓度比原平衡也大 |
| B.达到平衡后,升高温度,既加快了正、逆反应的速率,又提高了NH3的产率 |
| C.达到平衡后,缩小容器的体积,既有利于加快正、逆反应速率,又有利于提高氢气的转化率 |
| D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,逆反应速率减小 |
下列有关工业生产的叙述正确的是( )
| A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
| D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
下列关于化工生产原理的几种叙述中,均符合目前工业生产实际情况的是( )
| A.石油是烃的混合物,石油工业中采用干馏的方法把石油分成不同沸点范围的产物 |
| B.氯气和氢气混合在光照条件下生成氯化氢,再用水吸收生成盐酸 |
| C.二氧化硫在接触室被氧化成三氧化硫,再在吸收塔内被水吸收制成浓硫酸 |
| D.合成氨工业中,由于氨易液化,N2、H2循环使用,所以总体来说氨的产率很高 |
化学工业是国民经济的支柱产业.下列生产过程中不涉及化学变化的是
| A.氮肥厂用氢气和氮气合成氨 | B.钢铁厂用热还原法冶炼铁 |
| C.硫酸厂用接触法生产硫酸 | D.炼油厂用分馏法生产汽油 |
下列使用化肥、农药的描述中正确的是( )
| A.高温多雨时比较适合施用钾肥 |
| B.长期施用硫铵会造成土壤板结 |
| C.石硫合剂必须与硫酸混合后才能施用 |
| D.草木灰可以和铵态氮肥一块施用 |
在接触法产生H2SO4的过程中,对“废气、废水、废渣、废热”的处理正确的是( )
①废气用氨水处理 ②污水用石灰乳处理 ③废渣用来造水泥或炼铁 ④设置“废热”锅炉产生蒸气来供热或发电
| A.只有①② | B.只有①③④ | C.只有①②③ | D.全部 |

 2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)