碘元素对人的健康非常重要。下面是从海带灰中分离出单质碘(I2)的流程图。
(1)过程①的实验操作名称是____________,____________。
(2)上述过程中,属于氧化还原反应的是_______,离子方程式为 。
(3)过程③的实验操作名称是___________和___________;在此过程中,可供选择的有
机溶剂是_______(填字母代号)。
| A.酒精 | B.CCl4 | C.苯 | D.醋酸 |
① ;
② ;
③ ;
④ 。(有几处填几处,不必填满,多填扣分。)
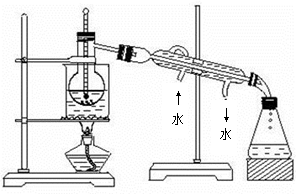
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| | 苯 | 溴 | 溴苯 |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了_______气体。继续滴加至液溴滴完。装置d的作用是_____ ___;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是____________________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必需的是________(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________ (填入正确选项前的字母)。
A. 25 mL B.50 mL C.250 mL D.500 mL
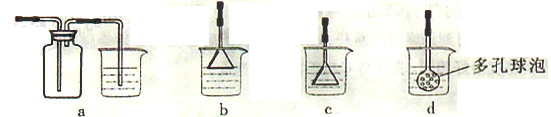
TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元素组成,与氢气的相对分子质量之比为120。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。其主要过程为在足量氧气流中将4.80 g TMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热装置等已略去,其他用品可自选)。
(1)将所选用的仪器(可重复选用)连接顺序由上到下依次填入下表,并写出该仪器中应加入的试剂的名称及作用。
| 选用的仪器 | 加入试剂 | 加入试剂的作用 |
| C | H2O2溶液与MnO2 | 产生氧气 |
| | | |
| | | |
| D | CuO粉末 | 将可能生成的CO转化为CO2 |
| | | |
| | | |
| | | |
(2)实验后称得A及以后的装置(均用A装置并假设每次吸收均是完全的)质量依次增加3.60 g、14.08 g、0.14 g,则TMB的分子式为__________________________。
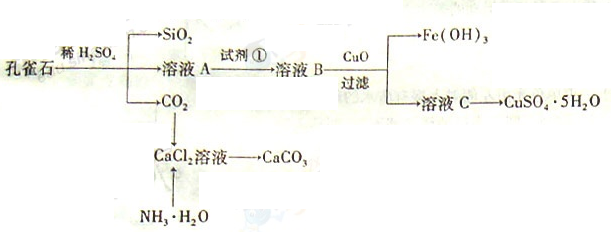
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下: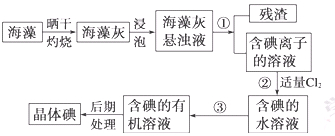
(1)指出操作③的名称: ;操作②中充入适量Cl2的目的是 。
(2)提取碘的过程中,可供选择的试剂是 ( )
| A.酒精 | B.四氯化碳 | C.汽油 | D.醋酸 |
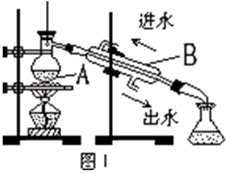
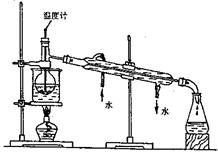
(3)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏。图I是某同学设计的蒸馏装置,图中明显的错误是 。
(4)有同学认为蒸馏时最好使用水浴加热,使用水浴的优点是: ;蒸馏结束,晶体碘聚集在 (填仪器名称)里。
(5) 实验③分离出来的废液中含有Cl–、SO42–,现只取一次试液,如何鉴别出Cl–、SO42–,依次加入试剂的为: 、 。
(6)某小组同学实验时需用到一定物质的量浓度的碘水溶液225mL,配制时需要的仪器除天平、玻璃棒、烧杯外,还需 、 。若摇匀时,发现液面低于刻度线,则配得溶液浓度(填偏大、偏小或无影响)。
实验室用乙醇和浓硫酸共热制取乙烯,常因温度过高而生成少量的二氧化硫,有人设计下列实验以确认上述混和气体中有乙烯和二氧化硫。
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:I ;II ;III ;IV (将下列有关试剂的序号填入空格内);
| A.品红溶液 | B.氢氧化钠溶液 | C.浓硫酸 | D.酸性高锰酸钾溶液 |
(3)使用装置Ⅱ的目的是 _________________________________________________ ;
(4)使用装置Ⅲ的目的是___________________________________________________;
(5)确证含有乙烯的现象是_________________________________________________。
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
| | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 2PCl3;2P+5Cl2 2PCl3;2P+5Cl2 2PCl5 2PCl5 |
| PCl3 | —112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
(一)制备:RU 图是实验室制备PCl3的装置(部分仪器已省略)

(1)仪器乙的名称____________。
(2)实验室用漂白粉加浓盐酸制备Cl2的化学方程式:_______________________ 。
(3)碱石灰的作用是____________________。
(4)向仪器甲中通入干燥Cl2之前,应先通入一 段时间的CO2,其目的是____________________。
(二)提纯:
(5)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过_________________(填实验操作名称),即可得到PCl3的纯品。
(三)分析:
测定产品中PCl3纯度的方法如下:迅速称取4.200 g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的0.1000 mol/L 20.00 mL 碘溶液,充分反应后再用0.1000 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗10.00 mL Na2S2O3溶液。
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应。
(6)根据上述数据,该产品中PCl3的质量分数为____________________ 。若滴定终点时俯视读数,则PCl3的质量分数_______(偏大、偏小、或无影响)