下列与金属腐蚀有关的说法正确的是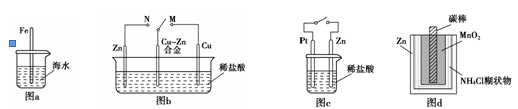
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu?Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
某小组为研究电化学原理,设计如下图装置。下列叙述不正确的是 ( )
| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 |
用铂电极电解某溶液一段时间,该溶液浓度增大而pH减小,该溶液是 ( )
| A.NaOH | B.CuCl2 | C.H2SO4 | D.CuSO4 |
下列有关物质的性质和该性质的应用均正确的是 ( )
| A.常温下浓硫酸与铝不发生反应,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
用气体传感器可以检测汽车尾气中CO的含量。传感器是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇?氧化钠,其中O2- 可以在固体介质NASICON中自由移动。下列说法正确的是
| A.燃料电池工作时,电极b作负极 |
| B.工作时,电流由负极通过传感器流向正极 |
| C.b电极的电极反应式为:O2+2H2O+4e-=4OH- |
| D.当消耗11.2L(标准状况下)CO时,理论上传感器中会通过NA个电子 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 +Pb+2H2SO4=2PbSO4+2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 | B.负极的电极反应式为:Pb+SO42--2e– = PbSO4 |
| C.PbO2得电子,被氧化 | D.电池放电时,溶液酸性增强 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法错误的是( )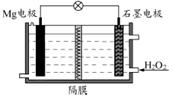
| A.Mg 电极是该电池的负极 |
| B.溶液中Cl-向石墨电极移动 |
| C.该装置中电子从Mg电极流向石墨电极 |
| D.H2O2在石墨电极上发生还原反应 |
不能用Fe+H2SO4=FeSO4+H2↑表示的是( )
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
| C.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| D.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
气态废弃物中的硫化氢可用电化学的方法转化为可利用的硫:配制一份电解质溶液,主要成分为:K4[Fe(CN)6](200 g/L)和KHCO3(60 g/L);通电电解,通入H2S气体。过程中涉及硫化氢转化为硫的总反应:2Fe(CN)63-+2CO32-+H2S=2Fe(CN)64-+2HCO3-+S,则下列说法不正确的是( )
| A.电解过程中的阳极反应为:[Fe(CN)6]2――e-=[Fe(CN)6]3- |
| B.电解过程中阴极附近溶液的pH降低 |
| C.电解过程中每处理l mol硫化氢气体,理论上转移电子2 mol |
| D.该处理方法理论上不需要补充电解质溶液 |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越
来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为xMg+Mo3S4  MgxMo3S4;在镁原电池放电时,下列说法错误的是
MgxMo3S4;在镁原电池放电时,下列说法错误的是
| A.Mg2+向正极迁移 |
| B.正极反应为:Mo3S4+2xe-=Mo3S42x- |
| C.Mo3S4发生氧化反应 |
| D.负极反应为:xMg-2xe-=xMg2+ |