已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )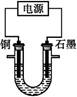
| A.铜电极连接电源正极 |
| B.黑色粉末X是铁粉 |
C.铜的相对原子质量的计算式是 |
D.石墨电极上发生的反应是4OH--4e- O2↑+2H2O O2↑+2H2O |
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2 CaO作电解质,利用右图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中正确的是( )
CaO作电解质,利用右图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛。下列说法中正确的是( )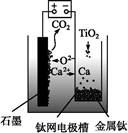
| A.由TiO2制得1 mol金属Ti,理论上外电路转移2 mol电子 |
B.阳极的电极反应为C+2O2--4e- CO2↑ CO2↑ |
| C.在制备金属钛前后,整套装置中CaO的总量减少 |
| D.若用铅蓄电池作该装置的供电电源,石墨电极应连接Pb电极 |
下图是一套电化学装置,对其有关说法错误的是( )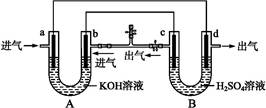
| A.装置A是原电池,装置B是电解池 |
| B.反应一段时间后,装置B中溶液pH增大 |
| C.a口若消耗1 mol CH4,d口可产生4 mol气体 |
D.a口通入C2H6时的电极反应为C2H6-14e-+18OH- 2C 2C +12H2O +12H2O |
关于下列说法中正确的是( )
A.用惰性电极电解熔融氯化钠的离子方程式为:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| B.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg |
C.下图为电解足量氯化钠溶液的装置,一段时间后两极收集到气体的体积之比为1∶1 |
| D.电解精炼铜时,相同时间内阴极析出铜的质量比阳极溶解铜的质量大 |
一种太阳能电池的工作原理如图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液。下列说法中不正确的是( )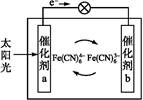
| A.K+移向催化剂b |
B.催化剂a表面发生的化学反应:Fe(CN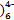 -e- -e- Fe(CN Fe(CN |
C.Fe(CN 在催化剂b表面被氧化 在催化剂b表面被氧化 |
D.电解质溶液中的Fe(CN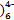 和Fe(CN 和Fe(CN 浓度基本保持不变 浓度基本保持不变 |
已知Fe2+与K3[Fe(CN)6]溶液反应呈蓝色。某同学进行如下图的实验,将左铁棒的上、下两端各联上一锌片,而在右铁棒中段联上一铜片(如图1),并将它们同时静置于含有K3[Fe(CN)6]及酚酞的混合胶质溶液中。经一段时间后,发现图中的甲、乙、丙、丁、戊、己等六区均有变化(如图2)。下列关于各区变化情况的判断,正确的是( )
| A.甲区呈现蓝色 | B.乙区呈现红色 |
| C.戊区产生Cu2+离子 | D.丁区产生Fe3+离子 |
下列与装置有关的说法中正确的是( ) 
| A.图a中,随着电解的进行溶液中H+的浓度越来越大 |
B.图b中,Al电极作电池的负极,电极反应为Al-3e- Al3+ Al3+ |
C.图c中,发生的反应为Co+Cd2+ Cd+Co2+ Cd+Co2+ |
| D.图d中:K分别与M、N连接,Fe电极均受到保护不会腐蚀 |
将下图所示实验装置的K闭合,下列判断错误的是
| A.盐桥中的K+移向乙池 |
B.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| C.b电极上的反应式为4OH-—4e-=O2↑+2H2O |
| D.片刻后可观察到滤纸a点变红色 |
图中乙是甲的电解池进行电解时的某个量(纵坐标x)随时间变化的曲线(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),则x表示( )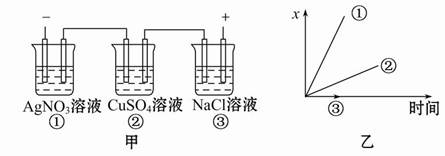
| A.各电解池析出气体体积总数的变化 |
| B.各电解池阳极质量的增加 |
| C.各电解池阴极质量的增加 |
| D.各电极上放电的离子总数的变化 |
串联电路中四个电解池分别装有0.5 mol·L-1的下列溶液,用惰性电极电解,连接直流电源一段时间后,溶液pH最小的是( )
| A.KNO3溶液 | B.NaCl溶液 | C.AgNO3溶液 | D.CuCl2溶液 |