题目内容
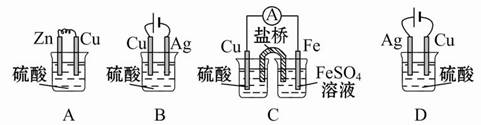
将下图所示实验装置的K闭合,下列判断错误的是
| A.盐桥中的K+移向乙池 |
B.电子沿Zn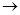 a a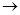 b b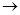 Cu路径流动 Cu路径流动 |
| C.b电极上的反应式为4OH-—4e-=O2↑+2H2O |
| D.片刻后可观察到滤纸a点变红色 |
B
解析试题分析:将装置中K闭合,该装置构成原电池,其中甲池中Zn是负极,电极上发生氧化反应,乙池中Cu是正极,发生还原反应,依次来判断;A、原电池中阳离子向正极移动,即向乙池移动,正确;B、电子沿Zn→a,在a、b上是溶液中的离子放电,电子不能直接由a→b,错误;C、硫酸钠润湿的滤纸是电解池,b是阳极,OH-放电发生氧化反应4OH-—4e-=O2↑+2H2O,正确;D、在a处是阴极,溶液中的H+ 得到电子,c(H+) 减小,c(OH-)增大,a处滤纸变红色,正确。
考点:原电池和电解池。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2(s)+Pb(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(I),根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e-=PbSO4↓ |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
用惰性电极实现下列电解实验,其说法正确的是
| A.电解稀硫酸溶液,实质上是电解水,故溶液的pH不变 |
| B.电解稀氢氧化钠溶液,阳极消耗OH-,故溶液的pH减小 |
| C.电解硫酸钠溶液,阴极和阳极析出产物的物质的量之比为2:1 |
| D.电解氯化铜溶液,通电一段时间后,向溶液中加入适量的CuO或CuCO3均可使电解液恢复到起始状态 |
以石墨做电极,电解1 mol/L下列物质的水溶液,下列表述正确的是
| A.若为盐酸,pH减小 | B.若为氢氧化钠溶液,pH减小 |
| C.若为硫酸钠溶液,pH不变 | D.若为氯化钠溶液,pH不变 |
实验发现,298 K时,在 FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如右图所示的原电池装置。下列有关说法中正确的是( ) 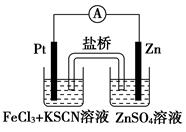
| A.该原电池的正极反应是:Zn-2e-=Zn2+ |
| B.左烧杯中溶液的红色逐渐褪去 |
| C.该电池铂电极上有气泡出现 |
| D.该电池总反应为:3Zn+2Fe3+=2Fe+3Zn2+ |
利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的是( )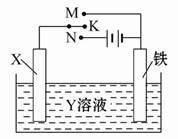
| A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法 |
| B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀 |
| C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 |
| D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
下列实验现象预测正确的是(双选) ( )。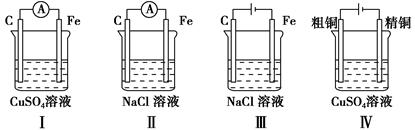
| A.实验Ⅰ:电流表A指针偏转,碳棒上有红色固体析出 |
| B.实验Ⅱ:电流表A指针偏转,铁极上有无色气体产生 |
| C.实验Ⅲ:碳棒上有无色气体产生,铁极上有黄绿色气体产生 |
| D.实验Ⅳ:粗铜溶解,精铜上有红色固体析出 |
下图是一套电化学装置,对其有关说法错误的是( )
| A.装置A是原电池,装置B是电解池 |
| B.反应一段时间后,装置B中溶液pH增大 |
| C.a口若消耗1 mol CH4,d口可产生4 mol气体 |
D.a口通入C2H6时的电极反应为C2H6-14e-+18OH- 2C 2C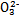 +12H2O +12H2O |